文章目录
NK细胞研究
NK细胞研究
NK细胞研究概述
NK细胞基础生物学
自然杀伤(NK)细胞可选择性地溶解细胞,而无需事先活化。NK细胞属于天然淋巴细胞(ILC),天然淋巴细胞作为天然免疫系统的一部分,对于免疫监视和随后的宿主防御病毒感染和癌细胞至关重要。在人体中,NK细胞占循环淋巴细胞的8-20%;在实验室的近交系小鼠中,NK细胞占脾脏和骨髓淋巴细胞的2-5%[1,2]。与其他淋巴细胞(包括B细胞、T细胞和自然杀伤T(NKT)细胞)不同,NK细胞不表达克隆性B细胞受体或T细胞受体/ CD3ε复合体等抗原特异性受体。相反,NK细胞以抗原非依赖性方式(通常不会生成免疫记忆或长期保护性免疫)发挥作用。近期研究表明,NK细胞是癌症治疗的潜在治疗靶点。
NK细胞来源于CD34+淋巴祖细胞。据估计,NK细胞的半衰期大约为7~10天,它占人类外周血淋巴细胞总数的10-15%,也存在于脾脏、肝脏、肺、骨髓和淋巴结中,它们通过与树突状细胞(DC)的相互作用发挥关键的免疫调节功能。NK细胞是第1组固有淋巴样细胞的典型成员,聚集在一起,以获得分泌IFN-γ的能力。终末分化的NK细胞缺乏B(CD19)和T(CD3)淋巴细胞的表型标记,CD56是NK细胞特征的标志。
通常,通过其大小,以及含有穿孔素和颗粒酶的细胞质颗粒将其区别出来,这是NK细胞杀伤活性的重要效应。
NK细胞根据CD56的表达水平被进一步区分:dim 和 bright。CD56 dim是一种完全成熟的NK细胞,占外周血NK细胞的90%,主要起介导细胞毒性的作用;另一方面,CD56 Bright是一种不成熟的细胞因子产生的细胞,其溶细胞反应有限。NK细胞缺乏基因重排抗原受体,但仍能识别和直接裂解异常转化的细胞,无需事先致敏。这是通过在NK细胞表面表达的一组成熟而独特的受体来实现的,这些受体通过与被感染和恶变的细胞上的配体相互作用而激活细胞裂解活性。虽然配体仍未完全表征,但NK细胞受体的分类依据其作用:激活、抑制和混合功能。它们还表达细胞因子受体,包括IL-2受体(R)、IL-4、10、12、15、18和21-R,以及TGF-β受体(TGF-β-R).下图概述了NK细胞活动的主要受体。

激活受体包括天然细胞毒性受体,由NKp30、44和46组成。NKp30识别带B7-H6肿瘤抗原,NKp44结合病毒血凝素和血凝素神经氨酸酶以及其他肿瘤相关配体。NKp 46抑制小鼠转移瘤生长。Fcγ-RIIIa(CD16)是另一种激活受体,可触发抗体依赖的细胞毒性(ADCC)。
抑制性受体包括CD161、CLRG1、PD1、TIM3、LAG 3、CD96和TIGIT。具有混合功能的NK细胞受体包括杀伤细胞Ig样受体(KTR)和NKG2受体:KIR2DS、KIR2B4和KIR3DS与其他具有抑制作用的KIR不同。
同样,NKG2A受体抑制NK活性,而NKG2D信号传导激活信号,通过与肿瘤细胞上选择性表达的特定应激诱导配体(MICA、MICB和病毒UL16结合蛋白)结合,启动细胞毒活性。
NK细胞抗肿瘤活性:肿瘤识别和细胞裂解活性
NK细胞对肿瘤细胞具有天然的杀伤作用,也是IFN-γ、TNF-α、粒细胞-巨噬细胞集落刺激因子(GM-CSF)等细胞因子和趋化因子的主要来源。这些细胞因子参与其他造血细胞的招募和功能,例如增强抗原特异性T细胞反应,以及与DC和中性粒细胞的调节交叉调节网络。
NK细胞一旦遇到肿瘤细胞,就会启动溶细胞颗粒的定向外吐,包括释放穿孔素和颗粒酶,分别穿透细胞质膜并触发凋亡。这些细胞被NK细胞认为是“非自我的”,因为它们的MHC-I的减少/缺乏,而MHC-I在身体几乎每一个健康的细胞上都有表达。这种选择性攻击可以通过一种创造的“耐受性”过程来实现,即成熟的NK细胞表达生殖细胞编码的抑制受体,识别正常细胞的MHC-I,并触发一个抑制信号(通过免疫受体酪氨酸基抑制基)来阻止对这些‘自我’细胞的酪氨酸激活信号。
当NK细胞遇到细胞异常缺乏MHC-I或MHC-I者减少时,抑制性受体不被激活,激活信号仍未被抑制,从而引发裂解攻击。建立“自我”耐受性的原因是“NK许可”过程,即在NK细胞功能发育过程中,NK细胞上的抑制受体与其同源的MHCⅠ类配体配对,从而赋予对自身抗原的耐受性。
这一过程与表达自MHCⅠ类特异性受体的功能能力强的NK细胞有关,而不表达这种受体的细胞没有获得许可,也不需要受到MHC I类的抑制,因为它们在功能上没有这个能力。了解这一过程与开发基于NK细胞的治疗有关。
研究还认为,在耐受过程之外,抑制性受体不仅对抗激活受体,而且通过自身识别抑制受体的发展,参与对成熟NK细胞识别自我的“教育”:在NK细胞成熟过程中,NK细胞随机表达个体抑制性KIR基因,直到有一种不同的抑制受体组合识别出MHC-I信号。人们提出了许多模型来解释这一过程。
另一种针对癌细胞的方法是通过CD 16受体(FCγRIIIA)在NK细胞上表达。活化后,NK细胞能有效地识别与癌细胞结合的IgG抗体的Fc部分,并通过ADCC溶解这些包被抗体的细胞。
NK细胞:激活适应性免疫系统的桥梁
在细胞毒性反应的同时,释放的细胞因子和趋化因子进一步吸引其他NK细胞、DC和T细胞。肿瘤坏死因子-α等促炎细胞因子通过NK细胞FASL与肿瘤细胞Fas复合物的相互作用诱导肿瘤细胞坏死,从而诱导靶细胞凋亡。其他趋化因子(如CCl 3、4、5和10)通过化学梯度将免疫效应细胞定向到肿瘤部位,而其他如IL-10和IL-6则在产生部位增强免疫活性。例如,通过释放CCL 5、XCL 1和XCL 2,NK细胞促进DC进入实体肿瘤。同样地,淋巴结中NK细胞的激活促进了IFN-γ的释放,通过吸收额外的免疫效应细胞,包括抗原提呈细胞(巨噬细胞和树突状细胞),诱导促炎性肿瘤微环境,最终驱动TH1免疫反应,动员T细胞进入淋巴结,并从CD8 T细胞分化为细胞毒性T淋巴细胞。最后,NK细胞通过攻击未成熟的DC和保留成熟的DC,以保证免疫应答的质量。
与NK细胞相关的肿瘤免疫逃逸的机制
NK细胞与MHC-I分子之间的关键相互作用是防止自身免疫破坏的重要机制,也是肿瘤细胞逃避免疫系统导致NK细胞失能的关键机制。对不同肿瘤类型的多项研究表明,当肿瘤内NKG2D激活的NK细胞相对于外周血中的比例较高时,对转移有积极的预后价值和风险预测。肿瘤细胞逃避NK细胞免疫监视的一种方法是将NK细胞与KIR受体结合后识别为自身的MHCⅠ类分子表达。其他的肿瘤逃逸方式也被描述,包括通过PDPD-L1的相互作用来抑制免疫反应,类似于T细胞抑制。NK2GD配体、MICA和MICB从肿瘤细胞表面脱落是肿瘤逃逸的另一个主要机制,同样,肿瘤细胞通过产生TGF-β和Kynurenine而进化出下调NK细胞NKG2D表达,也是一种策略。正是由于我们对这些逃逸机制的具体理解,我们才制定了新的、以NK细胞为基础的治疗策略。
肿瘤微环境和NK细胞抗肿瘤活性
TME在肿瘤细胞逃避NK细胞免疫监视中起着重要作用。它被认为是一种破坏正常血液供应和血管生成的环境,并通过基质、代谢和免疫抑制机制的激活而诱导低氧环境。这种缺氧破坏了NK细胞的多种功能,为肿瘤的扩张、生长和转移创造了有利的环境。微环境可通过肿瘤源因子、自噬调节杀伤、调节癌细胞代谢和肿瘤衍生小泡,如肿瘤细胞外显子和分泌的microRNAs等低氧状态下产生的微RNA,导致NK细胞功能受损。
缺氧是产生免疫抑制性TME的关键因素之一,低氧肿瘤细胞通过抑制NKG2D激活受体的表达和产生转化生长因子-β而产生细胞因子,这些细胞因子通过抑制NKG2D激活受体的表达和分泌而产生细胞因子,包括调节性T细胞(Treg)的上调。通过产生HIF1-α,MDSCs分化为肿瘤相关巨噬细胞,表现出M2反应,并从癌细胞中切割Fas配体,导致NK和CTL功能受损。此外,低氧环境允许癌细胞培养基质细胞,并通过转化生长因子-β或IL-6的产生将其激活为与肿瘤相关的成纤维细胞。这些细胞因子反过来抑制IL-2诱导的NK细胞活化受体的上调,从而降低NK细胞的细胞毒性和免疫监视。
除了创造一个免疫抑制环境外,缺氧还会破坏 NK 细胞的功能和细胞毒性。增加 TME 中的乳酸和腺苷。乳酸通过降低细胞外的功能而破坏 NK 细胞的功能pH值和腺苷升高导致抑制 IL-2 刺激的 NK 细胞释放 TNF - α ,并抑制NK 细胞的增殖和细胞毒性功能。此外,缺氧诱导的一氧化氮 (NO) 信号传导激活导致 MICA 脱落,这是一种重要的肿瘤逃逸机制,同时也导致 COX-2/PGE2 途径的解除调节。在许多腺瘤和癌细胞中发现 COX-2 过表达缺氧条件和 PGE2 的增加被发现直接抑制 NK 细胞的细胞毒性作用多激活受体的下调。此外,氧气和营养缺乏在穷人灌注环境导致自噬激活,从而摄取和降解 NK 细胞颗粒酶B释放。
最后,肿瘤细胞逃避研究的最新进展集中在肿瘤细胞来源的外显子和分泌的微RNA在TME中的作用[46]。含有转化生长因子-β、MICA或MICB的肿瘤外显子可降低NK细胞NK2GD激活受体的表达,减弱NK细胞的杀伤能力和增殖[47,48]。微RNA,特别是miR-210,在缺氧条件下被发现释放,并能诱导血管生成和肿瘤生长/转移。对microRNAs的更好理解可能被用来开发新的预后和/或治疗反应的生物标志物。
免疫抑制 TME 在阻止 NK 细胞激活方面特别重要,如上所述..
然而,NK 细胞在实体肿瘤中的疗效的另一个主要障碍与其肿瘤部位成功归巢有关。这一方面,特别是解释了成功地将体外实验转化成体内环境。前述趋化因子梯度的解除是阻止 NK 的主要机制细胞归巢到实体肿瘤部位。例如,已经证明异常的 EGFR-RAS 信号可以抑制产生 CCL27 ,阻止白细胞归巢皮肤肿瘤和加速小鼠肿瘤生长模型 。同样,通过活性氮对 NK 细胞招募的重要趋化因子 CCL2 进行亚硝基化在 TME 中的物种,降低了它吸收白细胞的能力,而改变的 CXCL 11 蛋白水解损害了结合并通过趋化因子的信号传递,最终减少淋巴细胞的迁移 。另一个挑战是适当的归巢和肿瘤浸润与不良的病理性血管生成有关,血管生成是一个实质性的屏障适当的 NK 细胞传递和细胞向肿瘤部位的外渗,并介导免疫抑制。
NK细胞和肿瘤干细胞
肿瘤干细胞(CSCs)是肿瘤中能够通过不对称细胞分裂自我更新的少数亚群。这些细胞是肿瘤细胞异质性的基础,这对目前的抗癌治疗方式提出了挑战,主要与实体肿瘤有关。CSCs对传统的癌症治疗具有抗药性,其治疗后的持久性可导致疾病复发,而其去分化状态使其能够转移和/或重新植入先前的靶向病变。一般来说,CSCs的特点是缺乏一致的表面标记。然而,正是由于缺乏/下调MHC-I的表达,首先引起了关于NK细胞在针对CSC的潜在用途方面的问题。这一观点在涉及结直肠癌和胶质母细胞瘤样本的一些研究中得到证实,在接受化疗的患者源性细胞系中检测到CSCs的富集,随后NK细胞有效地靶向CSCs。在一组全面而优雅的实验中,Ames等人。证明NK细胞如何优先靶向CSCs,利用NK细胞与多种人癌细胞株和分离的原癌标本共培养模型(自体和异体),以及NK在异种移植小鼠模型中的转移:这种优先靶向性CSCs是通过NKG2D激活受体的相互作用而产生的。从健康供者(用重组人白细胞介素-2培养)分离和扩增的NK细胞与患者来源的肿瘤细胞共同孵育时,流式细胞仪检测发现ALDHDim和ALDHbrightCSCs均有明显下降,后者表现出更高的敏感性NK 细胞治疗。同样,在皮下异种移植瘤模型中,瘤内注射激活的NK细胞后,CSCs(由ALDH和CD24的表达确定)明显减少,免疫荧光研究显示肿瘤内NK细胞浓度增加。在乳腺癌转移模型中,静脉注射体外激活的NK细胞可导致转移性肺肿瘤的肿瘤集落数量减少,肿瘤集落缩小。最后,静脉注射NK细胞处理小鼠原位胰腺癌模型,生物发光显像显示治疗组与未治疗组相比发光降低,支持NK细胞在体内靶向CSCs。流式细胞术和定量逆转录-聚合酶链反应(RT-PCR)显示NKG2D配体和Fas死亡受体在CSCs群体中的表达明显高于非CSCs,支持NK细胞活化受体配体和死亡受体在靶向CSCs中的作用。有关CSCs的类似工作也有报道,涉及儿童和青少年/青少年肿瘤,如骨肉瘤。
NK 细胞的另一种非细胞毒性作用最近被描述为“分裂无力”,NK 细胞与 TME 中的单核细胞和巨噬细胞相互作用,导致非能细胞不具有细胞毒性,而是分泌细胞因子,从而促进 CSCs 的分化,使它们对标准更加敏感。 CSCs 对肿瘤增殖、复发和转移的重要性他们对标准细胞毒性治疗的耐药性,靶向 CSCs 已成为肿瘤学的一个兴趣领域,为发展新的治疗方式开辟新的机会。
参考文献
Lopez-Soto A,. Cancer Cell 32(2), 135–154 (2017).
Fang M, J.Exp. Med. 207(11), 2369–2381 (2010).
Fauriat C,. Blood 115(11), 2167–2176 (2010).
Khalil Choucair,Future Oncol. (2019)
Kim S, Poursine-Laurent J, Nature 436(7051), 709–713 (2005).
Brodin P, . Blood 113(11), 2434–2441 (2009).
Kim S, Proc. NatlAcad. Sci. USA 105(8), 3053–3058 (2008).
Raulet DH, Nat. Rev. Immunol. 6(7), 520–531 (2006).
1.NK细胞——自带免疫记忆的天然免疫细胞
自然杀伤细胞(Natural Killer,NK)被视为天然免疫系统里的重要成员,具有快速产生效应细胞因子和杀死病毒感染或肿瘤细胞的能力。然而至今也愈来愈多的研究显示, 部份的NK细胞具有很强的适应环境变化能力及最终分化成生命周期长、高度功能的特殊细胞群,称为记忆或适应性NK细胞( memory or adaptive NK cells)。
长期以来,人类和许多哺乳动物的免疫系统主要分为两类:天然免疫和适应性免疫系统。前者主要是依靠NK细胞识别攻击非自身细胞。后者则是B细胞和T细胞能够对外来侵入者形成长期记忆,当再次遇到时就能直接快速地将其扼杀。然而,科学家们发现在小鼠体内,天然免疫系统的NK细胞可对接触过的抗原形成“记忆”,在不依赖B细胞和T细胞的适应性免疫中发挥作用。
NK细胞对抗原特异性回忆反应的首次证明是在半抗原诱导的接触超敏反应中,小鼠肝脏内的CXCR6+ NK细胞可介导抗原特异性接触超敏反应。记忆性NK细胞的特性也同样在巨细胞病毒(CMV)感染的小鼠模式中得到验证。当小鼠受到巨细胞病毒再次感染时,记忆性NK细胞会开始进行二次扩增、快速释放脱粒酶和细胞因子产生保护性的免疫反应;并为新生小鼠受到母体垂直感染巨细胞病毒时提供保护。这样独立于T细胞和B细胞的适应性免疫之外的记忆性NK细胞,也在灵长类动物模式中发现其存在。然而,记忆性NK细胞是否存在于人类免疫系统依然未解。
直到2019年,美国加州斯克里普斯研究所(Scripps Research Institute) Dr. Silke Paust团队利用“人源化”免疫系统的小鼠模型与人体试验发现:NK细胞在人体中也能形成抗原“记忆”的功能。
|
阅读原文:Human Natural Killer Cells Mediate Adaptive Immunity to Viral Antigens Rana Nikzad1,2,9, Laura S. Angelo1, Kevin Aviles-Padilla1,3, Duy T. Le1,4, Vipul K. Singh1, Lynn Bimler1,4, Milica Vukmanovic-Stejic5, Elena Vendrame6, Thanmayi Ranganath6, Laura Simpson6, Nancy L. Haigwood7, Catherine A. Blish6,8, Arne N. Akbar5, and Silke Paust1,2,3,4,9 |
脾脏和肝脏含有组织特异性NK细胞
Dr. Silke Paust团队首先建立一个“人源化”免疫系统的小鼠模型(BLT (BM, liver, and thymus) humanized mouse model),人类免疫细胞取代了小鼠的免疫细胞。利用质谱流式细胞技术(CyTOF mass cytometry)与多参数的流式细胞术(Flow Cytometry)对BLT小鼠分离出的脾脏和肝脏进行NK细胞图谱分析。相比外周血单个核细胞(PBMC)内的NK细胞,脾脏和肝脏内含有丰富的CD56hi/CD16lo NK细胞,并表达CXCR6、T-bet、Emos…等不同特异性蛋白,揭示着组织特异性的NK细胞功能与特性不同于外周血内的NK细胞。由表现图谱分析,脾脏和肝脏NK细胞具有组织特异性并表现小鼠记忆NK细胞标记CXCR6、淋巴结归巢能力、细胞毒性效应和产生IFN-γ。类似结果也在人体内相应器官组织(脾脏和肝脏)的NK细胞获得。

BLT小鼠的脾脏和肝脏具有组织特异性人NK细胞
Adapted from Nikzad et al., Sci. Immunol. 4, eaat8116 (2019)
NK细胞拥有“记忆”能力
研究中,将BLT小鼠注射HIV包膜蛋白疫苗,再从小鼠的肝脏和脾脏中提取NK细胞并分别培养一段时间。再让这些细胞暴露于遞呈HIV包膜蛋白、流感病毒H1N1蛋白片段、与惰性蛋白(ovalbumin)的DC细胞。结果显示,接触过HIV抗原的小鼠NK细胞在遇到呈现HIV蛋白的DC细胞组会起作用,但不响应惰性蛋白组,对流感病毒组响应亦有限。这些结果支持了”NK细胞能够回忆起曾与病原体的接触”的假设。更有趣的是,这项结果仅在BLT肝脏提取出的NK细胞验证,而脾脏的NK细胞并未表现出该特性。

人类的肝脏NK细胞介导抗原特异性和疫苗依赖性杀伤
Adapted from Nikzad et al., Sci. Immunol. 4, eaat8116 (2019)
人记忆性NK细胞长期存在体内
为了探究NK细胞在人体内是否也具有适应性免疫与长生命周期,Dr. Silke Paust团队进行延迟型超敏反应(delayed-type hypersensitivity, DTH) 人体试验;招募年龄在22-65岁之间在孩童时期患有水痘-带状疱疹病毒 (varicella zoster virus, VZV)的健康成年受试者,并给他们注射水痘病毒的糖蛋白。在注射部位,水痘患者的皮肤会产生类似水疱(blister-like)的反应。一旦水疱形成,可从水疱分离出NK细胞。分析显示,与机体其它地方的NK细胞不同,这些NK细胞表现NK细胞成熟杀伤性标记CD107,表示正在对抗原进行杀伤作用。这群活跃的NK细胞也并非是旁观者免疫细胞 (bystander immune cells),在皮肤的水疱部位被升高的细胞因子或趋化因子招募而来;因为细胞因子和趋化因子信号本身不会触发NK细胞介导的杀伤。且在表型和功能上与供体匹配的PBMC来源的NK细胞截然不同。显示在最初感染宿主数十年后,它们迅速进入VZV-STA的攻击位点,这表明NK细胞在人类的长期抗原特异性回忆反应中发挥作用。

人类NK细胞介导的免疫记忆是长寿的
Adapted from Nikzad et al., Sci. Immunol. 4, eaat8116 (2019)
记忆性NK细胞可帮助开发有效新型疫苗
“天然免疫细胞也带有免疫记忆”颠覆了以往的二元化认知: 渭径分明的天然免疫与适应性免疫。虽然NK细胞如何辨识区分抗原与自身细胞而形成免疫记忆的机制仍有待进一步研究,但经由这项研究带来了一种可能性:疫苗接种策略有望被开发用于诱导记忆性NK细胞。在未来,了解NK细胞如何形成适应性记忆,或许可帮助研究人员开发更有效的新型疫苗。
2.人 NKT/γδ Tcell markers
Human
| Pan markers |
γδ Tcell | NKT |
| CD3 | 分泌因子 GM-CSF● Granzyme B IFNγ● IL-4● IL-5● IL-17A● Perforin TNFα●
|
分泌因子 IL-4↑● IL-10↑● IL-13↑● IFNγ↑● TNFα↑● |
| 细胞表面 CD5● CD16● CD27● CD28● CD45RA● CD56● CD57● CD62L● CD69 CD70↑● CD107a● CD314(NKG2D) TCR γδ● TCR Vδ1● TCR Vδ2● TCR Vδ3● |
细胞表面
CD4● CD8● CD16 CD56 CD69 CD160 TCR Vα24○ |
|
| Intracellular/transcription factor PLZF Id2 |
↑=Upregulated ↓=Downregulated ○=Key marker ●=Subset
人全血13色免疫表型分析
B细胞、T细胞亚群、NK细胞和髓系细胞免疫表型分析

抗体组合
| 染料 | Excitation(nm) | Emission(nm) |
| Pacific Blue | 405 | 440/50 |
| Pacific Green | 405 | 512/25 |
| Pacific Orange | 405 | 603/48 |
| FITC | 488 | 530/30 |
| PerCP-Cy5.5 | 488 | 695/40 |
| PE | 561 | 685/16 |
| PE-Cy7 | 561 | 780/60 |
| APC | 637 | 670/14 |
| Alexa Fluor 700 | 637 | 720/30 |
| APC-Cy7 | 637 | 780/60 |
3.人 NK/ILC markers
Human
| NK | ILC1 | ILC2 | ILC3 | LTi |
| 分泌因子 Granulysin Granzyme A Granzyme B Granzyme K Granzyme M IFNγ IL-10 Perforin TNFα
|
分泌因子
CCL3(MIP-1α) IFNγ
|
分泌因子 IL-4 IL-5 IL-9 IL-13 Amphiregulin |
分泌因子
IL-17A● IL-17AF● IL-17F● IL-22● |
分泌因子 IL-17 IL-22 LTβ TNFβ(LTα) |
|
细胞表面 CD11b CD16 CD56○ CD69↑ CD94 CD122 CD161 CD244○ CD226 CD314(NKG2D) CD335(NKp46) CD336(NKp44)● CD337(NKp30) CD158 family KLRG1● TIGIT● |
细胞表面 CD56 CD103 CD183(CXCR3) CD335(NKp46) CD336(NKp44) CD337(NKp30) Linneg |
细胞表面 CD56 CD103 CD183(CXCR3) CD186(CXCR6) CD199(CCR9) CD278(ICOS) CD294(CRTH2) IL-25R(IL-17RB) IL-33R(ST2) Linneg TSLP receptor
|
细胞表面 CD56● CD117○ CD127(IL-7Rα)○ CD335(NKp46)● CD336(NKp44)● CD337(NKp30)● IL-23R Linneg |
细胞表面 CD7 CD25 CD117○ CD127(IL-7Rα)○ CD161 CD196(CCR6) CD252(OX40L) IL-23R MHCⅡ |
| 胞内/转录因子 E4BP4 Eomes GATA-3 Id2 Runx1 T-bet TOX
|
胞内/转录因子 Id2 T-bet |
胞内/转录因子 Arginase-1 GATA-3 Gfi1 Id2 RPRα TCF1 |
胞内/转录因子 AHR Id2 RORγt T-bet● TCF1● |
胞内/转录因子 AHR Id2 RORγt Runx1 TOX |
↑=Upregulated ↓=Downregulated ○=Key marker ●=Subset
人全血13色免疫表型分析
B细胞、T细胞亚群、NK细胞和髓系细胞免疫表型分析

抗体组合
| 染料 | Excitation(nm) | Emission(nm) |
| Pacific Blue | 405 | 440/50 |
| Pacific Green | 405 | 512/25 |
| Pacific Orange | 405 |
603/48 |
| FITC | 488 | 530/30 |
| PerCP-Cy5.5 | 488 | 695/40 |
| PE | 561 | 685/16 |
| PE-Cy7 | 561 | 780/60 |
| APC | 637 | 670/14 |
| Alexa Fluor 700 | 637 | 720/30 |
| Alexa Fluor 700 | 637 | 780/60 |
4.小鼠 NKT/γδ Tcell markers
Mouse
| Pan markers | γδ Tcell | NKT |
| CD3 | 分泌因子
Granzyme B IFNγ IL-4● IL-5● IL-17A● Perforin TNFα●
|
分泌因子
IL-4↑● IL-10↑● IL-13↑● IL-17↑● IL-22↑● IL-21↑● IFNγ↑● TNFα↑●
|
| 细胞表面 CD25↑● CD27● CD28● CD44● CD45R(B220)↑● CD45RB● CD62L● CD69↑● CD71↑● CD103 CD122● CD127(IL-7Rα)● CD150● CD196(CCR6)● TCR γδ● IL-1R1● NK1.1(on C57BL/6)● TCR Vδ1● TCR Vδ4● TCR Vδ5● TCR Vδ6● TCR Vδ7● |
细胞表面
CD4● CD8● CD44↑ CD49b● CD94● CD160 CD183(CXCR3) CD184(CXCR4) CD186(CXCR6) CD314(NKG2D)● DX5 Ly-49● NK1.1(on C57BL/6) TCR Vα14○ |
|
| 胞内/转录因子 Eomes RORγt● T-bet● |
胞内/转录因子 PLZF Egr2 HEB Hobit |
↑=Upregulated ↓=Downregulated ○=Key marker ●=Subset
5.小鼠 NK/ILC markers
Mouse
| NK | ILC1 | ILC2 | ILC3 | LTi |
| 分泌因子
Granzyme A Granzyme B Granzyme K IFNγ IL-10 Perforin TNFα |
分泌因子 CCL3(MIP-1α) IFNγ
|
分泌因子 IL-4 IL-5 IL-9 IL-13 Amphiregulin |
分泌因子
IL-17A● IL-17AF● IL-17F● IL-22● |
分泌因子
IL-17 LTβ TNFβ(LTα) |
|
细胞表面 CD11b CD16 CD25 CD49b(DX5)○ CD94 CD122 CD161c(NK1.1) CD226 CD314(NKG2D) CD335(NKp46)○ Ly-49 family TIGIT |
细胞表面 CD103 CD183(CXCR3) CD335(NKp46)○ Linneg Ly-6A/E(Sca-1) |
细胞表面 CD25 CD117 CD127(IL-7Rα) CD184(CXCR4) CD186(CXCR6) CD199(CCR9) CD278(ICOS) CD294(CRTH2)○ IL-25R(IL-17RB)○ Ly-6A/E(Sca-1) IL-33R(ST2) TSLP receptor |
细胞表面 CD117 CD127(IL-7Rα)○ CD196(CCR6)○ CD335(NKp46)● IL-23R Linneg |
细胞表面 CD4 CD25 CD117 CD127(IL-7Rα)○ CD185(CXCR5) CD186(CXCR6) CD196(CCR6) IL-23R MHCⅡ |
| 胞内/转录因子 E4BP4 Eomes GATA-3 Id2 Runx1 T-bet TOX
|
胞内/转录因子 Id2 T-bet |
胞内/转录因子 Arginase-1 GATA-3 Gfi1 Id2 RPRα○ TCF1 |
胞内/转录因子 AHR Id2 RORγt T-bet● TCF1● |
胞内/转录因子 AHR Id2 RORγt○ Runx1 TOX |
NK1.1 (CD161)在C57BL/6, FVB/N和NZB小鼠NK细胞和T细胞亚群中表达,但是小鼠AKR, BALB/c, CBA/J, C3H, DBA/1, DBA/2, NOD, SJL和129不表达。
NKp46 (CD335)表达在小鼠BALB/c, SJL, CBA/CA, C57BI/6, NOD, DBA/2和B6.129 NK细胞上。
6.快速分选NK细胞的利器
自然杀伤(NK)细胞是一种表达多型性受体的稀有淋巴细胞,在先天免疫系统起着至关重要的作用。通常通过流式细胞分选或免疫磁珠分选的方法将NK细胞分选出来,为此北京诺为生物代理的加拿大STEMCELL Technologies提供了独特的NK细胞分选技术:RosetteSep全血分选NK细胞和EasySep磁珠分选NK细胞,RosetteSep全血分选NK细胞技术实现了更加快速、简捷有效的分选NK细胞。
NK细胞分选方法

RosetteSep优势
(1)无需磁极、分离柱和特殊仪器;
(2)负选出的细胞未经标记,可立即用于下游应用;
(3)减少人工操作时间,降低细胞流失。

RosetteSep+SepMate= 一步法直接从全血中25分钟分离高纯度细胞亚群。
EasySep细胞富集试剂盒可以从新鲜或者冻存的外周血单个核细胞(PBMC)、白膜层细胞等样本中获得高纯度、高回收率的NK细胞。EasySep利用四聚体复合物(TAC)技术,将细胞与EasySepTM磁珠相交联,然后通过EasySep磁极作用,使目的细胞与非目的细胞分离开,从而分选出目的细胞。
EasySep优点:
(1)简单:无需分选柱和分选柱清洗,避免了柱子堵塞的问题;
(2)快速:分选时间短,无柱子堵塞问题,节省样本,细胞活性高;
(3)高纯度:细胞纯度可高达95%以上。

?如何选择合适的NK分选试剂

7.NK细胞的分离和纯化
该方案用于阴性富集NK细胞,利用生物素化抗体标记非NK细胞,再用Anti-Biotin 超顺磁纳米微珠结合被标记的非NK细胞。当细胞悬液置于磁场中时,包括像 NKT 细胞这样的非NK细胞都滞留在磁场中,从而将NK细胞分选出来,富集分选的NK细胞不受任何干扰,保持原有的生理功能,可用于下游的细胞培养及其他细胞生物学功能实验。
01.人NK细胞富集分选 |
|||
0101.PBMC分离 |
|||
|
|
|||
所需试剂 |
操作流程 |
||
Septube-15密度梯度离心管(PBM,#601115)Septube-50密度梯度离心管(PBM,#601150)Lymphoprep淋巴细胞分离液(PBM,#LSB1077)
D-PBS without Ca 2+ and Mg2+ for cells(PBM,#201050)
|
1.将淋巴细胞分离液通过隔板中心的孔注入 SepTube管。 注入分离液的体积请参考下表。 |
||
Septube™密度梯度离心管 |
起始样本(mL) |
密度梯度离心液(mL) |
|
15 |
0.5-5.0 |
4.5 |
|
50 |
4.0-17.0 |
17.0 |
|
2.抗凝血用等体积 D-PBS 稀释,混合均匀。如:5 mL 抗凝血用 5 mL D-PBS 稀释。3.保持 SepTube管垂直,通过血清移液管将稀释的样品沿 管壁加入管中。样 品将会和隔板上方的分离液混合,但不会影响分离效果。注:样品也可以直接倒入 SepTube®管中,但要小心避免样品通过隔 板中央的小孔直接进入隔板下方的分离液中。4. 在开启离心机制动器的情况下,室温 1200×g 离心 10 分钟。注:如果样品在体外超过 24h 以上,建议离心 20 分钟以上。离心力(g)和转速(rpm)转换公式:
注:rpm:每分钟转速;RCF:相对离心力;Radius:离心机转子半 径(cm)5. 离心完成后,可以将最上层不含细胞的 D-PBS 稀释液吸出弃掉,或者直接将包含 MNCs 的上层稀释液直接倒入新的无菌离心管中。请勿倒置 SepTube ®管超过 2 秒,以免底层红细胞倒出。注:离心后,SepTube®隔板上表面可能存在少量红细胞,但这些少量的红细胞不会影响下游实验和细胞分离效果。如果 SepTube®隔板上表面发现有较多的红细胞,可能是由于采血时间较长引起的,此时可以继续 1200×g 离心 10 分钟,以减少红细胞的残留。6. 向分离的 MNCs 中添加 0.5-1 倍体积 D-PBS (2μM EDTA) + 2% FBS,室温 300×g 离心 8 分钟洗涤细胞。注:为去除分离 MNCs 中的血小板,可以关闭离心机制动器,室温120×g 离心 10 分钟洗涤 MNCs。建议彻底清洗单个核细胞,去除血小板,以获得最佳细胞分选效果。 |
|||
0102.人NK细胞分选(无柱) |
|||
|
ImunoSep免疫磁珠分选试剂盒(#710710)分离人NK细胞流程 |
|||
所需试剂 |
操作流程 |
||
ImunoSep™人NK细胞富集分选试剂盒(PBM,#710710)MAGNISORT MAGNET(PBM,#602005)ImunoSep™ Buffer(500mL)(PBM,#604050)5mL流式管(12x75mm)(corning,#352058) |
1. 用适当体积的ImunoSepTM Buffer重悬细胞,调整细胞浓度至1×108/mL(每 100 μL细胞悬液中含 1×107细胞),制备单细胞悬液。注意:细胞必须是单细胞悬液。如有必要,进行涡流震荡或移液管以移除团块,然后再继续细胞分选。2. 在12×75mm,5 mL流式管中放置所需数量的细胞,但不超过2×108细胞。3. 每100 μL细胞添加 20 μL分选试剂A。通过涡旋混匀或利用1 mL Tip吹打5次混匀。在室温下孵育10分钟。4. 加入ImunoSepTM Buffer至4 mL,洗涤细胞,然后在室温下以300×g离心5分钟。5. 弃去上清液,用 ImunoSepTM Buffer重悬细胞至其初始体积。6. 每 100 μL细胞添加10 μL分选试剂B。利用1 mL Tip吹打5次或涡旋仪震荡混匀。在室温下孵育5分钟。注意:分选试剂B在添加到细胞悬液前,必须用1mL Tip混合均匀,以确保最佳性能。7. 添加 ImunoSepTM Buffer至2.5 mL。用1 mL Tip吹打3次混合均匀,请勿涡旋混匀。8. 将盛有细胞悬液的5 mL流式管插入磁极中,使流式管底部通过磁极底部孔道,直至接触到工作台面。在室温下静置5分钟。9. 保持流式管在磁极中,将磁极和流试管一同拿起,快速将上清液倾倒入 15 mL 无菌离心管中。流式管倒置时长不可超过2秒,随即将其恢复到直立位置。注意:请勿弄脏或摇动磁极中倒置的流式管,以免降低分选细胞的纯度。10.从磁极中取下含有非NK结合细胞的流式管,再重复步骤7至9,共进行2次分离。将两部分游离于细胞悬液中的细胞汇集在15 mL离心管中。注意:此步骤可提高细胞回收率,若细胞量足够实验使用,此步可省略。11. 从磁极中取下含有非NK结合细胞的流式管并丢弃。未标记游离的人NK细胞收集在15 mL离心管中,供下游实验使用。12. [可选]:为获得最大纯度,可将步骤 11 中未结合的细胞以300×g离心5分钟。弃上清液 , 加入2.5 mL ImunoSepTM Buffer。通过1 mL Tip混合细胞,并转移到新的 12×75 mm,5 mL 流式管中。重复步骤 8 至 9 进行额外纯化。从磁极中取下含有非 NK 结合细胞的流式管并丢弃。未标记游离的人 NK 细胞收集在 15 mL 离心管中,供下游实验使用。 |
||
流式检测 |
|||
|
ImunoSep免疫磁珠分选试剂盒(PBM,#710710)分离人NK细胞的流式检测结果利用APC标记的人 CD3 单克隆抗体和PE标记的人CD56单克隆抗体标记细胞,对分选前(左)或分选后(右)的细胞进行流式分析。 |
|||
所需试剂 |
操作流程 |
||
D-PBS without Ca 2+ and Mg2+ for cells(PBM,#201050)CD3 Monoclonal Antibody (OKT3), APC(Thermo,#17-0037-42)CD56 Monoclonal Antibody (MEM-188), PE(Invitrogen,#MHCD5604)流式缓冲液(PBM,#222026)5mL流式管(12x75mm)(corning,#352058) |
1.将获得的PBMC和NK细胞分别悬浮于DPBS缓冲液中,制备成1x107胞/mL的单细胞悬液。2.两支流式管中分别加入50μL PBMC细胞悬液和50μL NK细胞悬液。3.将5μL CD3-APC抗体和5μL CD56-PE抗体混合于流式染色缓冲液中,使检测终体积达到100μL(例如,50μL细胞加入50μL抗体混合液)轻轻涡旋以混合均匀,同时还需设定单染管和对照管,以调节电压,去除荧光补偿干扰。4. 2-8℃或冰上避光孵育至少30分钟。5.每支流式管加入2mL流式细胞缓冲液洗涤细胞。室温400-600xg离心5分钟,弃上清。6.重复步骤5.7.用适量的流式细胞缓冲液重悬细胞。8.使用流式细胞仪,运用单染管和对照管调节合适电压后分析样本。 |
||
0103.人NK细胞分选(有柱) |
|||
所需试剂 |
操作流程 |
||
NK Cell Isolation Kit human(Miltenyi,#130-092-657)ImunoSep™ Buffer(500mL)(PBM,#604050)MACS分选架(Miltenyi,#130-042-303)MiniMACS分选磁极(Miltenyi,#130-042-102)MS分选柱(Miltenyi,#130-042-201)
MidiMACS分选磁极(Miltenyi,#130-042-302)LS分选柱(Miltenyi,#130-042-401) |
非特殊说明该试剂盒用于从人外周血单个核细胞(PBMC)中分离NK细胞。通过使用偶联生物素的抗体和NK细胞微珠混合物进行标记,非NK细胞,即T细胞、B细胞、干细胞、树突细胞、单核细胞、粒细胞和红细胞等非目的细胞可被标记去除。1.准备单细胞悬液并计数。2.40μL buffer重悬107细胞,细胞数目多时,可按比例调整体积。3.按107细胞加入10μL NK Cell Biotin-Antibody Cocktail,混匀,2-8℃孵育5分钟。4.按107细胞加入30μL buffer.5.按107细胞加入20μL NK Cell MicroBead Cocktail,混匀,2-8℃孵育10分钟.6.将LS或MS分选柱置于磁性分选架,分选柱种类可根据下表选择 |
||
分选柱 |
最大标记细胞量 |
最大上柱总细胞量 |
|
MS |
107 |
2x108 |
|
LS |
108 |
2x109 |
|
7.润洗分选柱,MS分选柱500μL buffer润洗,LS分选柱3mL buffer润洗,当分选柱无液滴滴落时,将孵育的细胞悬液转至分选柱,收集含未标记细胞的流出液(即富集的NK细胞)。8.加适量buffer洗涤分选柱,MS分选柱500μL buffer洗涤,LS分选柱3mL buffer洗涤,流出液可与第7步流出液合并一起,即为最终获得富集的NK细胞。9.(可选)从磁性分选架上取下分选柱,并将其放在合适的收集管上。 取适量的缓冲液(MS分选柱1mL,LS分选柱5mL)到分选柱上,用分选柱塞推入分选柱,即可冲洗出磁性标记的非NK细胞。 |
|||
流式检测 |
|||
|
NK Cell Isolation Kit human(Miltenyi,#130-092-657)分离人PBMC中NK细胞。用CD56-PE 和CD3-FITC对细胞进行荧光染色。基于散射信号和碘化丙啶(PI)将细胞碎片和死细胞排除。 |
|||
02.小鼠NK细胞富集分选 |
|||
0201.小鼠脾细胞单细胞悬液制备 |
|||
所需试剂 |
操作流程 |
||
40μm细胞筛(Stemcell,#27305)ImunoSep™ Buffer(500mL)(PBM,#604050) |
对于小鼠脾细胞,建议使用 40 μm 细胞过滤网,过滤单细胞悬液去除碎屑或细胞组织团块,以获得最佳试剂盒分选性能。建议使用 ImunoSepTM Buffer(含 EDTA) |
||
0202.小鼠NK细胞分选(无柱) |
|||
|
ImunoSep免疫磁珠分选试剂盒(#720710)分离小鼠NK细胞流程 |
|||
所需试剂 |
操作流程 |
||
ImunoSep™小鼠NK细胞富集分选试剂盒(PBM,#720710)MAGNISORT MAGNET(Novo,#602005)ImunoSep™ Buffer(500mL)(PBM,#604050)5mL流式管(12x75mm)(corning,#352058) |
1. 用适当体积的 ImunoSepTM Buffer重悬细胞,调整细胞浓度至1×108/mL(每100 μL 细胞悬液中含 1×107细胞),制备单细胞悬液。注意:细胞必须是单细胞悬液。如有必要,进行涡旋振荡或用移液管移除团块,然后再继续细胞分选。2. 在12×75mm,5mL流式管中放置所需数量的细胞,但不超过2×108细胞。3. 每100 μL 细胞悬液添加20μL分选试剂A。通过涡旋仪混匀或利用1mL Tip吹打5次混匀。 在室温下孵育10分钟。4. 加入 ImunoSepTM Buffer至4mL,洗涤细胞,然后在室温下以300×g离心5分钟。5. 弃去上清液,用ImunoSepTM Buffer重悬细胞至其初始体积。6. 每100 μL细胞添加20 μL分选试剂B,利用1mL Tip吹打5次或涡旋仪震荡混匀。在室温下孵育5分钟。注意:分选试剂B在添加到细胞悬液前,必须用1mL Tip 混合均匀,以确保最佳性能。7. 添加分选缓冲液至2.5mL。用1mL Tip吹打3次混合均匀,请勿涡旋混匀。8. 将盛有细胞悬液的5mL流式管插入磁极中,使流式管底部通过磁极底部孔道,直至接触到工作台面。在室温条件下静置5分钟。9. 保持流式管在磁极中,将磁极和流式管一同拿起,快速将上清液倾倒入15 mL无菌离心管中。流式管倒置时长不可超过2秒,随即将其恢复到直立位置。注意:请勿晃动或摇动磁极中倒置的流式管,以免降低分选细胞的纯度。10. 从磁极中取出含有结合非 NK 细胞的流式管,再重复步骤7至9,共进行2次分离。将两部分游离于细胞悬液中的细胞汇集在15mL 离心管中。注意:此步骤可提高细胞回收率,若细胞量足够实验使用,此步可省略。11. 从磁极中取出含有结合非NK细胞的流式管并丢弃。未被标记游离的小鼠NK细胞收集在15mL离心管中,供进行下游实验使用。 |
||
流式检测 |
|||
|
ImunoSep免疫磁珠分选试剂盒(#720710)分离小鼠NK细胞的流式检测结果利用 APC-eFluor 780 标记的小鼠 CD3e 单克隆抗体和 APC 标记的小鼠NK1.1 单克隆抗体标记细胞,对分选前(左)或分选后(右)的细胞进行流式分析。 |
|||
所需试剂 |
操作流程 |
||
CD3 Monoclonal Antibody (UCHT1), APC-eFluor 780, eBioscience™(invitrogen,#47-0038-42)NK1.1 Monoclonal Antibody (PK136), APC, eBioscience™(invitrogen,#17-5941-81)流式缓冲液(PBM,#222026)5mL流式管(12x75mm)(corning,#352058) |
1.将获得的脾细胞和NK细胞分别悬浮于DPBS缓冲液中,制备成1x107细胞/mL的单细胞悬液。2.两支流式管中分别加入50μL脾细胞悬液和50μL NK细胞悬液。3.将5μL CD3 APC-eFluor780抗体和5μL NK1.1 APC抗体混合于流式染色缓冲液中,使检测终体积达到100μL(例如,50μL细胞加入50μL抗体混合液)轻轻涡旋以混合均匀,同时还需设定单染管和对照管,以调节电压,去除荧光补偿干扰。4.2-8℃或冰上避光孵育至少30分钟。5.每支流式管加入2mL流式细胞缓冲液洗涤细胞。室温400-600xg离心5分钟,弃上清。6.重复步骤5.7.用适量的流式细胞缓冲液重悬细胞。8.使用流式细胞仪,运用单染和对照管调节合适电压后分析样本。 |
||
0203. 小鼠NK细胞分选(有柱) |
|||
所需试剂 |
操作流程 |
||
NK Cell Isolation Kit mouse(Miltenyi,#130-115-818)ImunoSep™ Buffer(500mL)(PBM,#604050)Pre-Separation Filters(Miltenyi,#130-041-407)MACS分选架(Miltenyi,#130-042-303)MiniMACS分选磁极(Miltenyi,#130-042-102)MS分选柱(Miltenyi,#130-042-201)
MidiMACS分选磁极(Miltenyi,#130-042-302)LS分选柱(Miltenyi,#130-042-401) |
非特殊说明该试剂盒用于从小鼠脾细胞悬液中分离NK细胞。 非NK细胞,即T细胞、树突状细胞、B细胞、粒细胞、巨噬细胞和红细胞等通过使用生物素偶联抗体和抗生物素微珠的混合物间接磁性标记。通过去除磁性标记的细胞,可以分离出高纯度的未标记NK细胞。1. 准备小鼠脾单细胞悬液,细胞悬液可先用30μm Pre-Separation Filters过滤,以防堵塞分选柱,计数。2. 300xg 10分钟离心,彻底去除上清液。3. 40μL buffer重悬107细胞,细胞数目多时,可按比例调整体积。4.按107细胞加入10μL NK Cell Biotin-Antibody Cocktail,混匀,2-8℃孵育5分钟。5.按107细胞加入2mL buffer,300xg 10分钟离心,彻底去除上清液。6.按107细胞加入80μL buffer,加入20μL Anti-Biotin Microbeads,混匀,2-8℃孵育10分钟.7.将LS或MS分选柱置于磁性分选架,分选柱种类可根据下表选择 |
||
分选柱 |
最大标记细胞量 |
最大上柱总细胞量 |
|
MS |
107 |
2x108 |
|
LS |
108 |
2x109 |
|
8.润洗分选柱,MS分选柱500μL buffer润洗,LS分选柱3mL buffer润洗,当分选柱无液滴滴落时,将孵育的细胞悬液转至分选柱,收集含未标记细胞的流出液(即富集的NK细胞)。9.加适量buffer洗涤分选柱,MS分选柱500μL buffer洗涤,LS分选柱3mL buffer洗涤,流出液可与第8步流出液合并一起,即为最终获得富集的NK细胞。10.(可选)从磁性分选架上取下分选柱,并将其放在合适的收集管上。 取适量的缓冲液(MS分选柱1mL,LS分选柱5mL)到分选柱上,用分选柱塞推入分选柱,即可冲洗出磁性标记的非NK细胞。 |
|||
流式检测 |
|||
|
|
|||
8.NK细胞培养扩增
据报道,多种细胞因子组合被广泛应用于NK细胞的体外扩增。IL-2和IL-15的联合应用已经作为体外扩增NK细胞的经典方案,IL-2是重要的诱导NK细胞增殖的细胞因子,通过激活各种激酶通路,增加NK细胞活性,促进NK细胞增殖;IL-15可以上调NK细胞表面受体的表达,同时促进CD56+细胞的扩增。除此之外,近年来发现其它细胞因子同样可以调节NK细胞的活性以及分化。IL-12 p70可以诱导激活,刺激细胞毒杀伤以及INFγ和TNF的产生; IL-7可以促进NK细胞分化和诱导产生细胞毒性淋巴细胞的标志蛋白;IL-18能够上调NK细胞的细胞毒性,从而提高NK细胞的杀伤活性。通常,使用RPMI1640添加细胞因子进行NK细胞的体外扩增,但是,不同细胞因子组合,对于NK细胞体外扩增会有不同的影响,对K562细胞的杀伤也有着明显的差异。因此对于同一个实验,不同的的细胞因子组合会导致实验重复性差,而且添加细胞因子也相对费力。而无需额外添加细胞因子的完全培养基可完美克服这些缺点。
一. 主要材料和试剂
货号 |
名称 |
130-114-429 |
NK MACS CD Medium |
900105 |
人AB血清 |
|
Human IL-2 |
|
|
Human IL-15 |
|
|
14-8159 |
Human IL-15 Recombinant Protein, eBioscience™ |
|
Human IL-7 |
|
|
Human IL-12 p70 Carrier-Free Recombinant Protein, eBioscience™ |
|
|
IL-15 |
|
|
IL-18 |
|
|
IL-21 |
二.培养基的准备
- 2-8℃条件下融化NK细胞培养添加物。
- 加入1% NK细胞培养添加物到NK细胞基础培养基中。例如,在100 mL基础培养基中加入1 mL添加物。
- 加入5% AB血清,混匀。该培养基为完全培养基。
注意:仅仅准备3周的用量即可。完全培养基储存在2-8℃时最多可用3周。不要冻存。
- 使用前加入150/mL 的IL-2。此培养基为扩增培养基。
三. MNC或NK细胞的制备
- 3%乙酸的亚甲基蓝进行有核细胞计数。
原理:乙酸破坏红细胞和白细胞的细胞膜,而白细胞的细胞核被染成蓝色,通过对细胞核计数,确定有核细胞数量。3%乙酸溶液将破坏细胞膜,同时保留完好的细胞核。亚甲基蓝染色将使细胞核更容易观察。应在细胞加在乙酸溶液中约10 分钟内进行有核细胞的计数。
- 用含有3%乙酸的亚甲基蓝稀释20 μL样本。(将骨髓、脐血、动员后外周血来源的MNC稀释50到100 倍,外周血来源的稀释20到40倍。如果有核细胞数量较高,可能需要更高的稀释倍数)。
例如:对于50 倍稀释,将20 μL 细胞加入980 μL 含亚甲基蓝的3%乙酸中。
- 充分混匀稀释的样本。
- 用酒精清洗计数池和盖玻片,然后用无屑纸巾擦干,准备血细胞计数板。
- 将盖玻片小心地放在计数池上。
- 用移液器或毛细管吸取稀释后的样本,填满计数池,不能溢出或不足。
- 从血细胞计数板的一个计数池开始,使用手持式计数器或类似设备计数至少两对角1 mm 方格中的有核细胞。计数另一对角计数池相同数量的方格。如果细胞在边缘,采用计下不计上,计左不计右原则。记录细胞总数并计算每个方格的平均数。如果方格的细胞数不足10个,应制备浓度更高的悬液。


图1 Neubauer 血细胞计数板。九个大方格的边长都是1 mm,深度为0.1 mm。
- 血细胞计数板盖玻片覆盖的位置有9个方格,总体积为0.1 mm3(或10-4 cm3,相当于10-4 mL ),试用下列公式计算细胞总数:
每 mL细胞数=每个方格的平均基数×稀释倍数×104
细胞总数=每 mL细胞数×起始体积
- 用5-10倍体积的完全培养基清洗细胞,300x g离心10分钟。弃上清。
- 扩增培养基重悬细胞至1 x106细胞 /mL。
四. NK细胞培养实验步骤
图2 NK细胞培养流程图
- 在24孔板中加入300 µL /孔细胞悬液 (细胞密度1×106细胞/mL)。
- 0-6天,切勿扰动细胞。
- 第7天
- 取出50 μL细胞进行细胞计数(台盼蓝拒染,进行活细胞计数)。
- 如果细胞密度小于1×106细胞 /mL,添加足够的新鲜NK扩增培养基。
- 如果细胞密度大于1×106细胞 /mL,添加足够的新鲜NK扩增培养基稀释细胞至细胞浓度到4–5×105 细胞/mL(例如,如果第7天的时候细胞密度为1.5×106 细胞/mL,在现有的250 μL培养体系里加入500 μL新鲜扩增培养基,使总体积达到750 μL,细胞密度为 5×105 细胞/mL)。
- 第10天
- 吸取50 μL细胞进行细胞计数(台盼蓝拒染,进行活细胞计数)。
ii.细胞中加入足够量的新鲜NK细胞扩增培养基使细胞密度为 4–5×105 细胞/mL.
- 第12天
- 吸取50 μL细胞进行细胞计数(台盼蓝拒染,进行活细胞计数)。
ii.细胞中加入足够量的新鲜NK细胞扩增培养基使细胞密度为 4–5×105 细胞/mL.
6.第14天
吸取50 μL细胞进行细胞计数和细胞分析(例如,细胞毒性检测)。
五. NK培养结果分析


图3 NK细胞的扩增可以以PBMC为起始细胞或者直接用分离的NK细胞作为起始细胞。使用NK MACS扩增培养基扩增NK细胞的效率其它培养基的3倍。
在添加5%AB血清和500 UI/mL IL-2下(A)PBMC(n=3)和(B)分离的NK细胞(n=3)的扩增倍数
参考文献
- Klingemann HG , Martinson J. Ex vivo expansion of nature killer cells for clinical application[J]. Cytotherapy, 2004, 6(1): 15-22
- Pillet AH , Theze J, Rose T. Interleukin(IL)-2 and 15 have different effects on human nature killer lymphocytes[J]. Hum Immunol, 2011, 72(11):1013-1017
- Boyiadzia M, Memon S, Carson J, et al. Up-regulation of NK cell activating receptors following allogeneic hematopoietic stem cell transplantation under a lymphodepleting reduced intensity regimen os associate with elevated IL-15 levels[J]. Biol Blood Marrow Transplant, 2008, 14 (3):290-300
- Barao I, Hudig D, Ascensao JL. IL-15-mediated induction of LFA-1 is a late step required for cytotoxic differention of human Nk cells from CD34+ lin- bone marrow cells [J]. J Immunol, 2003, 171(2): 683-690
[5. 王晓梦,李玲,于津浦, 等。四种NK细胞体外扩增方案及其杀伤活性的比较.中国肿瘤生物治疗杂志,2013,20(3)
9.NK细胞杀伤功能
NK细胞通过直接识别靶细胞、释放穿孔素、NK细胞毒因子、TNF-α/β等杀伤因子杀伤靶细胞。
|
肿瘤特异性受体和细胞毒性融合蛋白的表达增强le NK细胞抗肿瘤活性。(A)自然杀伤(NK)细胞对肿瘤细胞的自然细胞毒性受刺激受体(NCRs)和NKG2D以及抑制性受体(如抑制性杀伤细胞免疫球蛋白样受体KIRs)的控制。(B)肿瘤相关细胞表面抗原特异性嵌合抗原受体(CAR)的表达有效地将NK细胞重定向到恶性细胞,并促进其细胞溶解活性而不依赖于内源性刺激受体的激活。(C)或者,NK细胞可以被修饰以表达靶向的细胞毒性嵌合体,如促凋亡丝氨酸蛋白酶颗粒酶B(GrB)融合到肿瘤细胞特异性配体或抗体片段。 这些分子与内源性颗粒酶和穿孔素一起储存在细胞毒性颗粒中。 当内源性NK细胞受体激活时,肿瘤靶向GrB与穿孔素一起释放,因此可以与自然细胞毒性机制合作杀死靶细胞。 尽管如此,通过内源性NK细胞刺激受体的信号不足可以重定向GrB变异体的释放。(D)这一问题可以通过肿瘤靶向GrB衍生物与CAR的共同表达来克服,该CAR确保NK细胞的激活,即使是通过其他耐药的癌细胞。 在这种情况下,CAR和靶向GrB可能指向相同或不同的肿瘤相关细胞表面抗原。 |
K562细胞是人白血病细胞系,其HLAⅠ型表达降低,而活化的NK细胞受体配体表达增高,使其特别易受NK细胞介导的细胞毒性作用的影响。将NK细胞与靶细胞(通常是K562细胞)共培养,然后通过检测靶细胞释放的酶或者用CAM、CFSE标记靶细胞,通过检测荧光,从而得出NK细胞的杀伤活性。

几种检测方法比如下:
|
检测方法 |
CCK8 |
WST-1 |
XTT |
MTT |
|
甲臜的水溶性 |
好 |
好 |
好 |
差 |
|
检测灵敏度 |
很高 |
高 |
高 |
高 |
|
检测时间 |
最短 |
较短 |
较短 |
较长 |
|
检测波长 |
430-490 nm |
420-480 nm |
420-480 nm |
560-600 nm |
|
细胞毒性 |
很低 |
很低 |
很低 |
高 |
|
细胞类型 |
任何细胞 |
任何细胞 |
任何细胞 |
不适合悬浮细胞 |
|
细胞形态 |
不变 |
不变 |
不变 |
完全消失 |
一. 主要材料和试剂
|
货号 |
名称 |
|
V13154 |
Vybrant™ MTT Cell Viability Assay |
|
88954 |
Pierce™ LDH Cytotoxicity Assay Kit |
|
CK04 |
Cell Counting Kit-8 |
|
eBioscience™ Calcein AM Viability Dye (UltraPure Grade) |
|
|
eBioscience™ Calcein AM Viability Dye (UltraPure Grade) |
|
|
eBioscience™ Calcein AM Viability Dye |
|
|
CFSE |
二. NK细胞杀伤
2.1 LDH释放检测杀伤
2.1.1乳酸脱氢酶 (LDH) 检测杀伤原理
乳酸脱氢酶 (LDH) 是活细胞胞浆内含酶之一。正常情况下,LDH不能透过细胞膜。当靶细胞受到效应细胞的攻击而损伤时,细胞膜通透性改变,LDH释放至培养基中。释放出来的LDH在催化乳酸生成丙酮酸的过程中,使氧化型辅酶Ⅰ(NAD+) 变成还原型辅酶Ⅰ(NADH)。后者再通过黄递酶还原硝基氯化四氮唑蓝(INT),形成有色的甲臢类化合物,在490nm处有一高吸收峰。利用读取的A值,经过计算即可得知NK细胞杀伤靶细胞的活性。甲臢的形成水平与释放到培养基中的LDH的数量成正比。

图1 LDH释放检测细胞杀伤活性原理
2.1.2 实验步骤
1. 调整效应细胞(NK细胞)密度至4.0×106 /mL、靶细胞(K562细胞)密度至1.0×105 /mL 。
2. 取96孔圆底培养板,每个样本做3次重复,按效靶比40:1、20:1、10:1加入效应细胞与靶细胞,每孔体积为100 µL。设置与实验孔相同数量的效应细胞自然释放对照孔,加培养基使每孔终体积为100 µL。设置与实验孔相同数量的靶细胞最大释放对照孔,加培养基使每孔终体积为90 µL(步骤4加10 µL裂解液)。设置与实验孔相同数量的靶细胞自然释放对照孔,加培养基使每孔终体积为100 µL。设本底(每孔100 µL NK细胞培养基)和体积纠正孔(每孔90 µL NK细胞培养基+10 µL 裂解液(步骤4加入))。
3. 在效应细胞和靶细胞自发释放孔中加入10 µL无菌、超纯水。

图 2 96孔板NK杀伤实验示意图
4. 将培养板放于37℃、5%CO2培养箱中孵育4小时。
5. 在最大孔和体积纠正孔中加入10 µL裂解缓冲液,孵育45分钟。
6. 250 x g 离心3分钟,每孔吸出50 µL上清液于相应平底培养板,避光加入50 µL反应底物,室温(15-25℃)避光30分钟,待各孔液体颜色转深时每孔加入50 µL终止液,轻拍培养板混匀。。
7. 将96孔板置于酶标仪检测490 nm和680 nm波长处的吸光值。为了确定LDH活性,应从490 nm处的吸光值中减去680 nm(来自仪器的背景信号)的吸光值(D)。
8. 为了计算准确,应该从实验平均值,效应细胞自发释放LDH对照值和靶细胞自发释放LDH对照值中减去本底对照平均值。体积纠正孔对照值应从靶细胞最大体积LDH释放对照中去除。
9. 用下列公式,计算每组E:T杀伤率%。
NK杀伤率(%)=(实验D值-效应细胞自然释放孔D值-靶细胞自然释放孔D值/(靶细胞裂解释放孔D值-靶细胞自然释放孔D值)×100%.
2.2 CCK8检测杀伤
2.2.1 CCK8检测杀伤原理
Cell Counting Kit-8(简称CCK-8)试剂可用于简便而准确的细胞增殖和毒性分析。其基本原理为:该试剂中含有WST-8【化学名:2-(2-甲氧基-4-硝基苯基)-3-(4-硝基苯基)-5-(2,4-二磺酸苯)-2H-四唑单钠盐】,它在电子载体1-甲氧基-5-甲基吩嗪鎓硫酸二甲酯(1-Methoxy PMS)的作用下被细胞中的脱氢酶还原为具有高度水溶性的黄色甲臜产物(Formazan dye)。生成的甲臜的数量与活细胞的数量成正比。该方法通常作为MTT法的替代方法。

图4 CCK8检测杀伤原理
2.2.2 实验步骤
1. K562细胞传代培养,取生长旺盛的细胞备用。用NK细胞培养液将细胞密度调为1×105 /mL。
2. 培养后的NK细胞调整细胞密度为1×106 /mL、 5×105 /mL、1×105/mL。
3. 将效靶比=10:1、5:1、1:1的NK细胞(效)、 K562细胞(靶)加入96孔圆底板,,实验组分别加入各效靶比的效、靶细胞 各50 µL/孔,均设3个复孔。同时设靶细胞孔(50 µL细胞悬液+50 µL培养基)及效应细胞(50 µL细胞悬液+50 µL培养基)孔作为对照孔。另加空白对照孔(NK细胞培养基100 µL / 孔),1孔。

图5 CCK8检测96孔板杀伤示意图
4. 震荡混匀,37℃、5% CO2培养箱孵育12小时。
5. 每孔加入10 µL CCK8 (5 mg/ml),充分震荡混匀,37℃、5% CO2培养箱继续孵育4小时。
6. 用酶标仪检测450 nm波长OD值。按下述公式计算杀伤率:
NK杀伤率( %)=[1-(效靶细胞孔OD值-效应细胞孔OD值) / 靶细胞孔D值]×100%
2.3 MTT检测杀伤
2.3.1 MTT检测杀伤原理
四甲基偶氮唑盐 (MTT) 是一种黄色的染料。活细胞线粒体中的琥珀酸脱氢酶能够代谢还原MTT,同时在细胞色素C的作用下,将淡黄色的MTT还原成蓝紫色、不溶于水的甲臜颗粒。该颗粒溶解后,其液体的吸光度OD值与活细胞数及细胞代谢活性呈正相关。因此吸光度OD值推测出活细胞的数目。由于死细胞中不含琥珀酸脱氢酶,因此加入MTT 不会产生甲臜。
2.3.2 实验步骤
1. K562细胞传代培养,取生长旺盛的细胞备用,用NK细胞培养液将细胞密度调为1×105 /mL。
2. 培养后的NK细胞调整细胞密度为5×106 /mL、2.5×106 /mL。
3. 将效靶比=50:1、25:1的NK细胞(效)、 K562细胞(靶)加入96孔圆底板, 实验组分别加入各效靶比的效、靶细胞各50 µL/孔,均设3个复孔。同时设靶细胞孔及效应细胞孔作为对照孔。另加仪器调零孔NK细胞培养基100 µL / 孔,1孔。

图6 MTT检测96孔板杀伤示意图
4. 置37℃、5% CO2培养箱培养4小时。
5. 每孔加入10 µL MTT (12 mM母液),继续孵育4小时。
注意:用1 mL PBS溶解5 mg MTT(组份A)配置12 mM的MTT母液。详见说明书。
6. 3000 rpm,离心10分钟,弃上清,每孔加DMSO 50 µL,充分混匀,10分钟内酶标仪检测570 nm波长A值。按下述公式计算杀伤率:
NK杀伤率( %)=[1-(条件OD值-效应细胞孔OD值) / 靶细胞孔OD值]×100%
2.4 CAM标记靶细胞检测杀伤
2.4.1 CAM标记靶细胞检测杀伤原理
Calcein-AM(CAM)是一种可以透过细胞膜的活细胞标记染料[10-11]。进入细胞后,细胞内酯酶会切断乙酰羟甲基酯(AM)的酯基,产生无法透过细胞膜的 Calcein 荧光染料。凋亡细胞和死细胞的细胞膜已被破坏,无法保留 Calcein。Calcein 的最佳激发波长为 495 nm,发射波长为 515 nm。
2.4.2 实验步骤

图 7 CAM标记靶细胞杀伤实验流程图
1. 杀伤检测前一天,复苏一支已经冻存的NK细胞并接种于NK细胞培养基中(培养的NK细胞忽略此步骤)。
2. 对于每个细胞杀伤检测试验,使用一种靶细胞系,需要6x105 NK细胞和3x105靶细胞。
注意:用NK细胞培养基将NK细胞和CAM染色的靶细胞(急性髓系白血病AML10和AML 13细胞)的密度分别调至1x106细胞/mL和1x105细胞/mL用于细胞毒性测定实验。另外,推荐的NK细胞数是专门针对方案中显示的E:T比例,如果使用较高的效:靶(E:T)比值相应增加NK细胞数(例如,对于40:1 E:T比使用4x106细胞/mL)。
3. 通过用NK细胞培养基稀释CAM(以1 mg/mL母液储存于DMSO中)制备CAM染色液。建议使用1:500,1:400,1:300, 1:200和1:100的稀释度对CAM进行稀释滴定,以达到最优浓度,使染色效果最佳。
4. 用1 mL CAM染色液重悬1 x 106 靶细胞。37℃,孵育1小时,期间时常对细胞进行晃动。
5. 重悬NK细胞至1x106 细胞/mL,然后在圆底96孔板前三孔(A1、B1、C1)添加200 µL NK细胞悬液。
6. 除达到最大体积的培养孔,在其它所有剩余的培养孔中添加100 μL完全培养基。
7. 在最大体积培养孔中加入100 μL 2% Triton X-100。
8. 通过每次转移100 μL细胞,进行NK细胞梯度稀释,从而达到5个梯度的E: T比例。混匀。从最后一个培养孔中去掉100 μL(E:T为0.3125: 1)。

图8 CAM标记染色靶细胞检测杀伤96孔示意图
9. CAM标记靶细胞1小时后,用NK细胞培养基洗涤细胞两次,400 x g 离心5分钟。
10.再次计数靶细胞,并重悬至1x105 细胞/mL。
11.每孔中加入100 μL(1x104细胞)靶细胞。100 x g离心1分钟以便效应细胞和靶细胞接触。
12. 37℃,5% CO2条件下孵育4小时。
13. 用100 μL移液管轻轻混匀培养物,使释放的CAM分布均匀,100 x g慢速离心培养板5分钟使细胞成团并将100 μL上清液小心转移至新的培养板,避免产生气泡。如果有气泡可以用针将气泡刺破。
14. 采用荧光读板器读板(激发波485 nm,发射波530 nm)或流式进行分析。最大体积培养孔中得到最大释放量,其余培养孔获得测试释放量。
根据公式[(测试释放量-效应细胞自发释放量)/(最大释放量-效应细胞自发释放量)x 100计算裂解百分比。
2.4.3 结果分析

图8 NK细胞对AML细胞的杀伤(用特异性裂解百分率表示NK细胞对AML的杀伤)
2.5 CFSE标记靶细胞检测杀伤
2.5.1 CFSE标记靶细胞检测杀伤
CFSE(5,6- carboxyfluorescein diacetate,succinimidyl ester) 即羟基荧光素二醋酸盐琥珀酰亚胺脂,是一种可穿透细胞膜的荧光染料,具有与细胞特异性结合的琥珀酰亚胺脂基团和具有非酶促水解作用的羟基荧光素二醋酸盐基团,这使得CFSE成为一种良好的细胞标记物。当CFSE以含有两个乙酸基团和一个琥珀酰亚胺酯功能基团的形式存在时,不具有荧光性质,而具有细胞膜通透性,能够自由进入细胞;而当其扩散进入细胞内后,内源的酯酶可将其乙酸基团水解,此种形式的CFSE分子具有很高的荧光活性,被激发能够产生绿色荧光,却不再具有膜通透性;同时,其含有的琥珀酰亚胺酯基团能与胞内的细胞骨架蛋白中的游离胺基反应,最终形成具有荧光的蛋白化合物。因此,当细胞进行分裂增殖时,具有荧光的胞质蛋白被平均分配到第二代细胞中,这样与第一代细胞相比,其荧光强度便会减弱至一半;以此类推,分裂得到的第三代细胞的荧光强度便会比第二代细胞再次减弱。这种现象可以在488nm的激发光下,采用流式细胞仪检测分析,通过检测到细胞荧光强度,从而进行细胞示踪和细胞增殖以及细胞毒性T 淋巴细胞 (CTL) 测定研究。
2.5.2 实验步骤
1. 用NK细胞培养基将预先培养好、生长旺盛的K562细胞重悬至细胞密度为1x106细胞/mL。
2. 将500 µL CFSE溶液加入到500 µL (5x105细胞)K562细胞悬液当中,上下吹打2-3次,混匀,使其终浓度达到0.5 µM。
注意:在500 µL NK细胞培养基中加入2 µL的CFSE 母液(5 mM)。涡旋,以便旋下瓶盖上的液体。然后将刚制备的50 µL CFSE 溶液加入950 µL NK细胞培养基进行1:20稀释,获得1 μM 的 2倍工作液。涡旋混匀,避光保存。
3. 5% CO2、37℃恒温箱中避光孵育10分钟。
4. 室温下,用10 mL的完NK细胞培养基避光终止反应10分钟。
5. 140× g,离心标记的K562细胞7分钟,弃上清并用1 mL NK细胞完全培养基重悬细胞。
6. 计数靶细胞并重悬使其终浓度为1x105细胞/mL。
7. 使用前,细胞可在室温下保存10分钟或者可将其置于37℃、5%CO2的恒温箱中直至使用。不要冷藏。
8. 使用96孔圆底培养板,按下列要求接种细胞(效应细胞:靶细胞,E:T):(1)E: T=5: 1+IL-2(阳性对照)、(2)E: T=5: 1、(3)E:T=2.5: 1、(4)1.25: 1、(5)E:T=0.625: 1、(6)靶细胞(K562死亡阴性对照)、(7)效用细胞、(8)靶细胞+吐温(K562细胞死亡阳性对照)。各设三个重复。

图9 CFSE标记染色靶细胞检测杀伤96孔示意图
9. 在(3)、(4)、(5)、(6)、(7)条件孔中各加入100 μL NK细胞完全培养基。
10. 在(1)、(2)、(3)条件孔中加入100 μL 效应细胞(NK细胞浓度5x105细胞/ mL)。通过依次稀释,在(4)-(7)条件孔中加入效应细胞。
i. 混合条件(3)孔,然后吸取100 μL加入条件(4)孔。
ii. 混合条件(4)孔,然后吸取100 μL加入条件(5)孔。
iii. 混合条件(5)孔,然后吸取100 μL加入条件(7)孔。条件(6)孔不加效应细胞。
11. 在条件(8)孔中加入100 μL制备的2倍体积0.2%吐温液(终浓度为:0.1%-吐温20),条件(8)孔中不加效应细胞。
12.在条件(1)孔中加入30 μL IL-2。在加入靶细胞悬液之前,应在效应细胞悬液中加入IL-2(终浓度为27 IU/mL)。
13. 在条件(1),(2),(3),(4),(5),(6),(8)孔中下加入100 μL 靶细胞(标记的靶细胞浓度为1x105细胞/mL)。
14. 混匀培养板,120 x g离心2分钟,以便使效应细胞和靶细胞充分接触。
15. 37℃,CO2恒温箱中孵育4小时。孵育结束后,将培养板置于冰上进行活细胞染色30分钟。
16. 将3 μL 5 μM SYTOX™ Red死细胞染色液加入到600 μLPBS中。
17. 在每个培养孔中加入50 μL稀释后的死细胞染色液,使终体积为250 μL,染色液终浓度为0.005 μM。
18. 进行流式细胞分析。
2.5.3 结果分析

图20 靶细胞检测设门
(A)最初的门设置在FITC-A/SSC-A点图中,CFSE细胞群为K562细胞为(B)死亡的K562细胞(细胞染色阳性群)在后面的APC-A/SCC-A点图中设门
参考文献:
1. 王晓梦,李玲,于津浦, 等。四种NK细胞体外扩增方案及其杀伤活性的比较.中国肿瘤生物治疗杂志,2013,20(3)
2. West, W. H., Cannon, G. B., Kay, H. D., et al. Natural cytotoxic reactivity of human lymphocytes against a myeloid cell line: characterization of effector cells [J]. J Immunol, 118 (1), 355-361 (1977)
3. 熊丹, 杨志刚,李庆华,等。高纯度CD3-CD56+CD16+NK细胞体外扩增技术的研究[J]。中国实验血液学杂志,2010,18(5):1310-1315
4. Srinivas S. Somanchi, Vladimir V. Senyukov, Cecele J. Denman,et al. Expansion, Purification, and Functional Assessment of Human Peripheral Blood NK Cells[J]. Journal of Visualized Experiments, 2011
5. Youn-Young Jang, Duck Cho, Sang-Ki Kim, et al. An Improved Flow Cytometry-Based Natural Killer Cytotoxicity Assay Involving Calcein AM Staining of Effector Cells[J]. Annals of Clinical & Laboratory Science, 2012, 42(1)
10.NK细胞疗法如何抗病毒
新型冠状病毒肺炎在各地快速蔓延,对人体最大的危害是攻击人的免疫系统,导致淋巴细胞下降,肺功能受损,危重病人甚至因为呼吸衰竭而死。同时也有很多病人因为免疫力下降,导致并发症,多器官衰竭而亡。目前无特效药可治愈新冠肺炎,在多方开发新药、新疫苗或临床试验老药新用的同时,开展NK细胞治疗提升患者免疫力是目前极为可行的治疗和预防策略。
开展NK细胞抗病毒临床研究
NK细胞治疗有别于药物或疫苗等传统治疗方法,主要是利用NK细胞的天然免疫杀伤能力,调动免疫系统主动杀伤侵入病毒及其感染的细胞,形成机体抵抗危险感染的首道防线。在早期一些研究中,NK細胞療法即顯示了抗病毒的有效潛力。而现今疫情紧急, 已有多项NK细胞治疗临床试验项目同时开展。
1. 美国Celularity和Sorrento Therapeutics制药公司:“应用CYNK-001治疗和预防新型冠状病毒的临床试验”;CYNK-001是一种脐带血来源的NK细胞产品,目前正进行临床试验NK细胞异体移植治疗急性骨髓性白血病与多发性骨髓瘤。
2. 河南省新乡医学院朱武凌教授: “脐带血NK细胞治疗冠状病毒感染重症患者的临床研究(201100311100)”;针对应急救治新型冠状病毒感染发病的患者和高危人群感染开展临床研究。
3. 广东省脐带血造血干细胞库: “脐血NK细胞联合脐血间充质干细胞用于治疗新型冠状病毒肺炎(COVID-19)的临床研究 (ChiCTR2000029817) ”;评估联合脐血分离出的NK细胞与间充质干细胞治疗新冠肺炎的安全性与有效性。
NK细胞抗病毒
自然杀伤细胞(natural killer cell,NK细胞),是除T细胞、B细胞之外的第三大类淋巴细胞,属于我们人体免疫第一道防线;不仅与抗肿瘤、抗病毒感染和免疫调解有关,甚至参与超敏反应和自身免疫性疾病的发生。
NK细胞有助于对病毒的早期免疫反应;不递呈抗原,但通过促炎细胞因子受体和生殖系编码激活受体感知环境中的危险/病原体信号。在与同源病毒配体结合后,这些受体参与了特定NK细胞亚群的特异性激活和群体扩张,部分地也再现了适应性淋巴细胞的某些特征。NK细胞的活化状态,执行细胞的脱粒、细胞因子释放和细胞杀伤功能均是抑制信号和活化信号综合的结果。

NK细胞:杀伤细胞活化受体(KAR)和杀伤细胞抑制受体(KIR)
NK细胞辨认病毒感染模式
在病毒感染期间,NK细胞使用各种策略来感知炎症信号。
a. 细胞因子IFN-α、IL-12、IL-15和IL-182在感染后早期大量表现,同时经由促炎细胞因子受体激活NK细胞与促使IFN-γ持续表现,介导抗病毒保护作用。
b. NK 细胞的一重要特性 “抗体依赖性细胞毒性 (antibody-dependent cellular cytotoxicity, ADCC)” :经由受体FcγRIII(CD16)结合被抗体包被的靶细胞(病毒感染细胞),从而激活NK细胞毒杀被感染细胞。通过这种识别模式,NK细胞对几乎所有病毒感染细胞都具有特异性。研究报告也指出特异性NK细胞亚群对流感病毒、单纯疱疹病毒1型(HSV-1) 和巨大病毒(CMV) 起到抗体依赖性细胞毒杀作用。
c. 当机体感染病毒时,NK细胞表达多种激活受体,如NKG2D、DNAM-1、NKp46和NKp3024。当NK细胞激活受体NKG2D的表达开始上调,可广泛监测应激细胞,使得NK细胞能够专门清除有害或不健康的宿主细胞。
d. 通过识别病毒颗粒片段或与病毒配体结合,激活特异性NK细胞受体,如KIRs与 NKG2C。如丙型肝炎病毒(HCV)NS3螺旋酶胜肽片段可激活NK细胞KIR2DS2受体。

NK细胞辨认病毒感染模式
Adapted from Natural killer cell specificity for viral infections. Hammer Q et al. Nat Immunol. (2018)
NK细胞作为重要的抗病毒细胞,之前研究表明NK细胞参与CMV、HSV、HCV、HIV病毒感染的免疫反应,甚至近期对人体危害大的SARS、ZIKA、登革热病毒都可发现NK细胞起到抗病毒作用。利用NK细胞免疫疗法可在免疫防御和免疫监控下,识别被感染的细胞,能快速分泌颗粒酶和穿孔素裂解细胞,并分泌促进炎症因子引起更广发的免疫应答,帮助患者改善机体平衡,达到快速有效抗病毒的效果。
脐带血赋予细胞治疗更多的可能性
为了遏止新冠肺炎疫情及获得有效治疗法,目前在中国临床试验注册中心(Chinese Clinical Trial Registry, ChiCTR)登记的临床试验高达116项;其中使用脐带血分离免疫细胞或间充质干细胞治疗新冠肺炎的临床研究就有以下五项:

以往脐带血被当做医疗废弃物;自1988年法国施行第一例脐血造血干细胞移植后,脐带血逐渐成为以造血干细胞进行骨髓重建的来源之一。此外,也可自脐带血分离单个核细胞、间充质干细胞与NK细胞应用于再生医学与免疫治疗中。
在不同NK细胞来源中,脐带血使用安全、便利。即使长期冷冻保存也不会影响分离出的NK细胞扩增能力与免疫功能。且脐带血来源的NK细胞更加年轻,增殖能力更强,靶向杀伤癌细胞的效率也更高,收集和冷冻保存更加便捷。目前有多项临床研究与试验正进行中,如加拿大McMaster University用于乳腺癌治疗,美国UCSF用于多发性骨髓瘤临床试验。美国MD Anderson癌症中心甚至利用脐带血开展CAR-NK临床研究。NK细胞用途强大,治疗前景可期。
NK MACS® 培养基------------------------------------------------------
美天旎NK MACS® Medium(货号#130-114-429)可支持不同来源的NK细胞在无滋养层下快速扩增,维持NK细胞完整功能(如细胞杀伤作用),并减少非NK细胞增生。同时亦提供NK MACS GMP级培养基供临床应用。 |
CryoMACS® 血液/细胞冻存袋--------------------------------------------------------------
|
||
|
产品 |
货号 |
推荐保存体积 |
|
CryoMACS Freezing Bag 50 |
200-074-400 |
10-20 mL |
|
CryoMACS Freezing Bag 250 |
200-074-401 |
30-70 mL |
|
CryoMACS Freezing Bag 500 |
200-074-402 |
55-100 mL |
|
CryoMACS Freezing Bag 750 |
200-074-403 |
80-190 mL |
|
CryoMACS Freezing Bag 1000 |
200-074-404 |
125-270 mL |
| 美天旎CryoMACS®冻存袋,独立无菌包装,GMP级质量保证;血液细胞冻存的正确选择。 | ||
11.NK细胞的体外扩增策略协助NK细胞临床应用
NK细胞无需预先致敏,便可通过快速激活一系列NK激活受体来识别和裂解肿瘤细胞。此外,异体NK细胞在造血干细胞移植(HSCT)中识别和杀伤急性髓性白血病(AML)中的作用,亦促进了基于自体/异体NK细胞,甚至是基因工程改造的NK细胞(如CAR NK),应用在高危癌症患者的免疫细胞治疗的开发;目前也已在1/2期临床试验中。随着人们对NK细胞研究不断深入,基于NK细胞的免疫治疗在新的抗肿瘤治疗策略中具有重要意义。

NK细胞的激活依赖于NK细胞表面表达的抑制性受体和激活性受体之间的平衡,它们与肿瘤细胞上的配体相互作用。Adapted from Cancer Immunol Immunother 2020 May;69(5):879-899.
NK细胞免疫治疗的细胞来源
以NK细胞为基础的过继性免疫治疗需要大量的细胞,其应用范围为患者每公斤体重需1×106—8×107 CD3-CD56+NK细胞 (即一个80kg的成人需要至少8x107NK细胞,并需多次回输)。此外,NK细胞在外周血中所占比例很低(5-15%),因此在用于过继性免疫治疗之前,有必要对其进行扩增。
自体或异体NK细胞用于移植,可从不同来源获得细胞:外周血单个核细胞(PBMC)、脐带血(UCB)、骨髓(BM)、诱导多能干细胞(iPSC)和细胞系。大量高纯度、高活性的NK细胞的扩增是其用于治疗的关键因素。NK细胞扩增可以纯化或富集的NK细胞抑或从单采血产品(如PBMCs)为起始材料。随后,扩增的NK细胞在最后阶段被纯化,通常是通过磁分选(CliniMACS® systems)来消除其他免疫细胞,如T或B细胞。这在异体造血干细胞移植至关重要,供者的异基因反应性T淋巴细胞会对患者产生副作用,如GvHD。因此,安全高效的生产方法是获得大量功能性NK细胞的关键,为NK研究和临床应用做好准备。
细胞因子诱导NK细胞增殖
体外扩增NK细胞,使用细胞因子是一种有效扩增NK细胞并提高其活性的方法,因为众所周知,它们介导NK细胞的增殖和活化。大量的细胞因子如IL-2、IL-15、IL-12、IL-18、IL-21和I型干扰素已被相继用于NK细胞的体外扩增。
IL-2可在短时间(24小时)内促进NK细胞的存活、激活和提高细胞毒性。IL-2刺激PBMCs可导致淋巴因子激活的杀伤细胞(lymphokine-activated killer, LAK)数量的增加,LAK由NK细胞和T细胞组成,对自体肿瘤细胞具有较高的杀伤能力。
IL-2和IL-15联合应用可促进NK细胞的增殖和活性,有利于NK细胞的激活。且只有IL-15 可以维持NK细胞在输注患者后的细胞溶解功能。IL-2和IL-15诱导NK细胞活化受体NKG2D、NKp44、NKp30和NKp46的表达,提高其对肿瘤细胞株的细胞毒性。IL-12也用于体外NK细胞培养,刺激NK细胞产生IFN-γ。IL-12、IL-15和IL-18联合作用可诱导细胞因子诱导的记忆样NK细胞(Cytokine-induced memory-like, CIML),是一种寿命长、细胞毒性高、分泌IFN-γ的细胞。CIML-NK细胞已在小鼠肿瘤模型中进行过继免疫治疗,并显示出抗黑色素瘤和淋巴瘤的良好效果。
辅助细胞和滋养层细胞协助NK细胞扩增
NK细胞的扩增需要多种生存、增殖和激活信号。因此,来自辅助细胞 (accessory cell)的刺激可以用来增强NK细胞的扩增,获得足够的细胞用于后续NK细胞治疗。过去文献显示,起始材料使用PBMC比使用纯化的NK细胞进行体外扩增,可获的更多数量的NK细胞,这表明PBMC中的其他非NK细胞为NK细胞的增殖提供了额外辅助。NK细胞与自体非NK细胞或生长失活的滋养细胞(如PBMC 或K562细胞系)共培养也也是一种策略,对NK细胞的活化和扩增有显著影响。尽管细胞系(ex. K562)共培养帮助NK细胞扩增取得了显著的效果,但这些用肿瘤细胞系进行扩增的方法需要建立一个主细胞库 (master cell bank),并遵循GMP严格的规定操作,以确保其在过继免疫治疗中的安全使用。
联合使用IL-2(500u/ml)和抗CD3单抗亦可幫助扩增健康供者和多发性骨髓瘤患者PBMC中NK细胞。值得注意的是,从PBMCs开始培养会导致CD3+T和NKT样(CD3+CD56+)细胞的扩增。因此,基于异体移植可能引起的T细胞介导的同种异体反应性,通过磁分选(CliniMACS® systems)来消除其他免疫细胞,以获得高纯度的NK细胞,是NK细胞治疗临床应用的关键。
|
NK MACS Medium |
|
- 优越的NK细胞扩增 - 减少非NK细胞生长,如B-, T- 和DC细胞 - 完全无异物添加 (Xeno-Free) - 提供GMP级NK MACS培养基供临床应用 |
美天旎 NK MACS Medium 提供了从各种来源,包括外周血单个核细胞(PBMC)或纯化的NK细胞,扩增和激活NK细胞的完美解决方案。配方成分明确的NK MACS Meidum能够扩增功能齐全的NK细胞,为任何下游应用做好准备。

IL-2和IL-15对NK细胞的高效扩增
使用NK MACS®培养(货号#130-1114-429)(辅以5% 人AB血清+IL2 500IU/mL+IL15140IU/mL)自纯化的NK细胞(5个不同来源的供者)中体外扩增NK细胞。经14天培养,NK细胞扩增倍率高达140倍。Acquired from Miltenyi in-house data.
12.自然杀伤细胞成熟的免疫研究
从健康献血者的全血中分离出自然杀伤细胞,并对其进行鉴定亚型。
该方案包括准备必要试剂和材料以及执行每个步骤的详细说明。
-
确定细胞数。将细胞悬液以300×g离心10分钟。
-
完全吸出上清液。将细胞重悬,每90 µL缓冲液最多可容纳106个有核细胞。
-
将每种抗体2 µL加入混合物中。
-
浮细胞在黑暗中于冰箱中(2-8°C)孵育10分钟。
-
通过添加1-2 mL缓冲液洗涤细胞,并以300×g离心10分钟。
-
上清液被完全吸出。
-
将细胞重悬于100 µL缓冲液中,然后在MACSQuant®Analyzer 10中进行样品采集。
流式数据
适应性或记忆性NK细胞。 分析了来自两个供体(CD3-CD56 +)的NK细胞的NKG2C表达。 随后对NKG2Chigh和NKG2C–亚型进行的门控表明存在KIR + CD57 +适应性或类似记忆的NK细胞。
以下是本方案每个步骤所需的试剂、仪器和耗材清单。这些产品仅供研究使用。
靶标 |
克隆号 |
荧光 |
货号 |
CD3 |
OKT3 |
eFluor 450 |
48-0037-42 |
CD56 |
CMSSB |
APC-eFluor 780 |
47-0567-42 |
CD57 |
TB01 (TBO1) |
PE-Cyanine7 |
25-0577-42 |
KIR2D |
NKVFS1 |
- |
MA1-82651 |
13.NK细胞研究方法
人NK细胞分离
人原代NK细胞可从外周血单核细胞(PBMC)中分离出来。从人血或外周血白细胞中分离PBMC,后续使用磁珠细胞分选(如Invitrogen Invitrogen Dynabeads Untouched人NK细胞试剂盒)NK细胞。流式细胞仪分选NK细胞也可以替代Invitrogen Dynabeads磁珠细胞分选方法。CD56和CD16是人NK细胞的特异性标志物,可以鉴别和分离不受其他淋巴细胞污染的NK细胞(图5)
NK细胞中的CD56表达水平决定表型特性。CD56Low/CD16Hi(CD56偏低/CD16偏高)NK细胞构成大部分循环性NK细胞;CD56HiCD16−/Low NK细胞占较小部分。CD56Hi NK细胞在IL-12的刺激下增殖并生成细胞因子。CD56Low NK细胞更具细胞溶解能力,当其活化受体参与时,可生成大量细胞因子。CD56Low NK细胞与CD56Hi NK细胞有所不同。NK细胞在活化和抑制受体表达方面属于异质性群体。
培养的NK细胞与体内分离细胞表现不同,并且表达不同的标志物。用IL-2培养的NK细胞将在CD57−CD56Low NK细胞亚群中诱导CD57表达。CD57+NK细胞高度成熟并具有多种特性,包括细胞毒性、对CD16刺激的敏感性、对细胞因子的较低反应性和增殖性。
图5.用CD56和CD16细胞标志物物鉴定并分离NK细胞。(1)提出分选方案,显示所有PBMC群体。(2)使用FSC和SSC对群体进行淋巴细胞门控,然后对淋巴细胞进行CD3负门控。(3)细胞分为CD56高和CD56低群体或CD56+正门控,并分为CD57高和CD57低群体。
小鼠NK细胞分离
小鼠NK细胞可通过Invitrogen Dynabeads磁珠细胞分选或流式细胞分选法从小鼠脾脏中分离出来。单细胞悬液可根据CD49b+、NK1.1+和CD3-进行分类。所有小鼠NK细胞应保存在添加有IL-2的培养基中。
NK细胞培养
人原代人NK细胞最多可培养8周。NK细胞可在添加有10%人AB+血清、2 mM Gibco CTS GlutaMAX-I、1 mM丙酮酸钠、100 U/mL rIL-2和25U/ml rIL-15的Gibco Advanced RPMI 1640培养基中保存。在植物血球凝集素(100ng/mL)存在的情况下,通过与受照射K562细胞共同培养6-9天来实现NK细胞扩增。NK细胞应用于CD56+/ NKG2D+高,并在含100ng/mL植物血球凝集素的RPMI完全培养基中与受照射K562共同培养。K562细胞应接受照射(6000拉德),以防止原代NK细胞增殖过程中的靶细胞增殖。
NK细胞的细胞毒性
人NK细胞毒活性的定量测定可使用靶细胞-K562来确定(图6)。靶细胞和NK细胞应在经细胞培养处理的培养板上共培养(如Thermo Scientific Nunc 96孔微孔板、经细胞培养处理的平底光学聚合物微孔板),在4℃温度下于Gibco Hanks缓冲盐水溶液(HBSS)中用5µg/mL纤连蛋白包被过夜。然后在每个孔中添加密度为1x105(K562)的靶细胞,并添加10ng/mL SDF-1α后于37℃下粘附1小时。然后用HBSS冲洗孔板。将HBSS中密度为5x105的NK细胞添加到每个孔中(一式三份),并在37℃下培养。细胞毒性可通过荧光成像用Invitrogen LIVE/DEAD Cell-Mediated Cytotoxicity Kit检测。细胞可使用EVOS Onstage培养室通过Invitrogen EVOS M7000成像系统进行成像,数据可使用Invitrogen Celleste图像分析软件进行分析。或者,可以使用高内涵分析平台对细胞进行成像和分析。
又或者采用流式细胞术,靶细胞可用Invitrogen CellTrace染料进行染色,然后添加Invitrogen SYTOX染料与效应性NK细胞一起培养。当NK细胞附着并杀死靶细胞时,细胞膜变为渗透式且SYTOX染料渗入,与核酸结合并发出荧光(可进行定量)。研究人员可使用Invitrogen Attune NxT流式细胞仪。
此外,也可使用以下流式细胞仪方案来评估NK细胞:OMIP-029:人NK细胞表型和OMIP-027:人自然杀伤细胞的功能分析。
图6.人NK细胞毒活性的定量检测。将K562靶细胞与绿色荧光膜染色剂DiOC18预培养,然后在添加红色荧光不透膜染料-碘化丙锭的情况下与效应细胞混合。存活和死亡的靶细胞均显示绿色荧光膜染色;细胞膜受损的靶细胞和效应细胞表现出红色荧光核酸染色;存活的效应细胞不发荧光。细胞使用EVOS Onstage培养室在Invitrogen EVOS M7000成像系统上成像。
细胞因子谱
虽然单个细胞因子能发挥一些作用,但NK细胞的完全活化、增殖、存活和效应功能通常需要不同细胞因子的组合。正调节NK细胞功能的细胞因子包括IL-2、IL-15、IL-12、IL-18、IL-21和IFG-g(主要由Th1细胞、巨噬细胞和树突状细胞生成)。相比之下,细胞因子IL-4、IL-5和IL-10(由Th2细胞分泌)或者IL-1β、IL-6、IL-10、IL-23、IL-35和TGFβ(由肿瘤细胞分泌)可抑制NK细胞功能。
表6:参与NK细胞活化、抑制和分泌的关键细胞因子。
| 活化 | 抑制 | 分泌 | |
|---|---|---|---|
| 细胞因子和趋化因子 | IL-2,IL-15,IL-12,IL-18和IL-21 IFG-g | IL-4,IL-5,IL-1β,IL-6,IL-10,IL-23,IL-35,TGF-β | IFN-γ,TNF-α,GM-CSF,IL-10,IL-5和IL-13,MIP-1α,MIP-1β,IL-8,RANTES |
| 其他因素 | 颗粒酶-A,-B,&-M,穿孔素 |
NK细胞的发育至少有五个不同的阶段,在这些阶段中各种细胞因子受体的表面表达表明不同的细胞因子与从一个发育阶段过渡到下一个发育阶段有关此外,随着使用基于自然杀伤细胞的癌症免疫疗法的新机会增加,了解细胞因子和免疫检查点抑制剂在肿瘤微环境中的作用及其对NK细胞的影响将变得至关重要。活化NK细胞可分泌多种细胞因子和趋化因子,其中包括GM-CSF、IL-10、IL-5、IL-13、IFN-γ、RANTES、TNF-α、MIP-1α、MIP-1β和IL-8(可使用免疫测定法测量)。此外,NK细胞上表达的免疫检查点标志物(如LAG-3、CD96、TIM-3、TGIT和PD-1)都能在血清或血浆中检测到。
多重免疫检测
| 物种 | 描述 | 分析物 | 货号 |
|---|---|---|---|
| 人 | Cytokine/Chemokine/Growth Factor Convenience 45-Plex Human Panel 1 | GM-CSF, IFN alpha, IFN gamma, IL-1 alpha, IL-1 beta, IL-1RA, IL-2, IL-4, IL-5, IL-6, IL-7, IL-8, IL-9, IL-10, IL-12p70, IL-13, IL-15, IL-17A (CTLA-8), IL-18, IL-21, IL-22, IL-23, IL-27, IL-31, LIF, SCF, TNF alpha, TNF beta, Eotaxin (CCL11), GRO alpha (CXCL1), IP-10 (CXCL10), MCP-1 (CCL2), MIP-1 alpha (CCL3), MIP-1 beta (CCL4), RANTES (CCL5), SDF-1 alpha, BDNF, EGF, FGF-2, HGF, NGF beta, PDGF-BB, PlGF-1, SCF, VEGF-A, VEGF-D | EPXR450-12171-901 |
| Immuno-Oncology Checkpoint 14-Plex Human ProcartaPlex Panel 1 | D27, CD28, CD137 (4-1BB), GITR, HVEM, BTLA, CD80, CD152 (CTLA4), IDO, LAG-3, PD-1, PD-L1, PD-L2, TIM-3 | EPX14A-15803-901 | |
| Immuno-Oncology Checkpoint 14-Plex Human ProcartaPlex Panel 2 | MICA,MICB,穿孔素,ULBP-1,ULBP-3,ULBP-4,精氨酸酶-1,CD73 (NT5E),CD96(可触觉),上皮钙粘蛋白,粘连蛋白-2,PVR,唾液酸结合免疫球蛋白样凝集素7,唾液酸结合免疫球蛋白样凝集素9 | EPX140-15815-901 | |
| 小鼠 | Immune Monitoring 48-Plex Mouse ProcartaPlex Panel | BAFF, G-CSF (CSF-3), GM-CSF, IFN alpha, IFN gamma, IL-1 alpha, IL-1 beta, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7, IL-9, IL-10, IL-12p70, IL-13, IL-15/IL-15R, IL-17A (CTLA-8), IL-18, IL-19, IL-22, IL-23, IL-25 (IL-17E), IL-27, IL-28, IL-31, IL-33, LIF, M-CSF, RANKL, TNF alpha, ENA-78 (CXCL5), Eotaxin (CCL11), GRO alpha (CXCL1), IP-10 (CXCL10), MCP-1 (CCL2), MCP-3 (CCL7), MIP-1 alpha (CCL3), MIP-1 beta (CCL4), MIP-2, RANTES (CCL5), Betacellulin (BTC), Leptin, VEGF-A, IL-2R, IL-7R alpha, IL-33R (ST2) | EPX480-20834-901 |
| Immuno-Oncology Checkpoint 7-Plex Mouse ProcartaPlex Panel 2 | CD137L (4-1BBL), CD152 (CTLA4), CD276 (B7-H3), CD80, PD-1, PD-L1, PD-L2 | EPX070-20835-901 | |
| Immuno-Oncology Checkpoint 4-Plex Mouse ProcartaPlex Panel 1 | BTLA、CD27、LAG-3、TIM-3 | EPX040-20830-901 |
14.NK细胞培养及NK细胞介导的杀伤
NK细胞培养
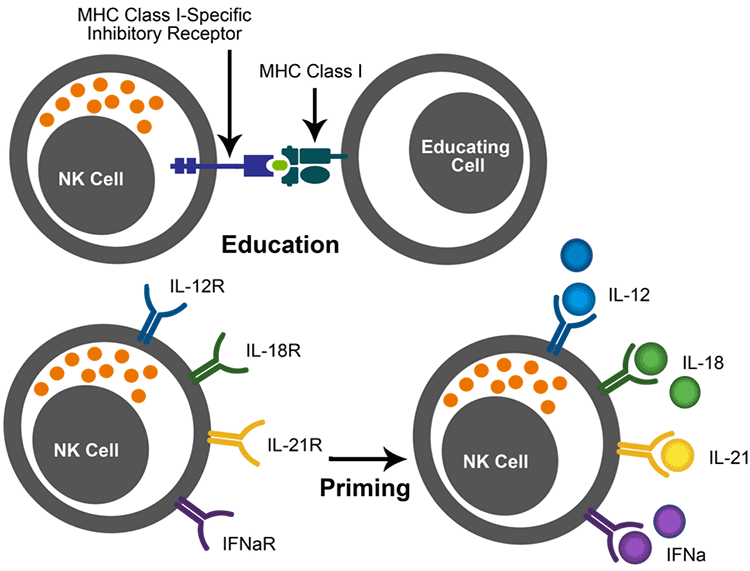
大多数正常健康细胞表达主要组织相容性复合体(MHC)I类分子,该类分子将这些细胞标志物视为“自身”。当NK细胞抑制性受体识别同源MHC I类分子时,NK细胞的细胞毒性功能关闭从而阻止其杀死这些细胞。为获得识别“非自身”靶细胞(具有低MHC I表达)的能力,必须教育NK细胞使用同源抑制性受体检测宿主MHC I类分子,这一过程也被称为调节或许可。
NK细胞还可通过细胞因子的启动过程来适应环境,此类细胞因子包括IL-2、IL-15(由树突状细胞转化而来)、IL-18、IL-12和IFNα(图1)。与邻近细胞相互作用后各种通路(抑制和活化)的整合控制着调节NK细胞活化的动态平衡,并决定了NK细胞是否活化以杀死靶细胞和生成细胞因子。天然免疫系统通常被认为缺乏免疫记忆能力;然而最新调查结果表明,一些NK细胞可以存活很长时间,并对异常细胞或病毒具有强大的回忆反应。
图 1.NK细胞教育。NK细胞与潜在靶细胞相互作用,通过正常健康细胞上表达的MHC I类分子的相互作用来学习什么是“自身”。此外,细胞因子(例如IL-12,IL-18,IL-21和IFNα)也可激活NK细胞。名词缩写表:MHC,主要组织相容性复合体;IL,白介素;IFN,干扰素。
NK细胞受体:活化和抑制活性
NK细胞能够在无需预先激活的情况下进行免疫监视和宿主防御,因此细胞表面受体的表达至关重要。NK细胞可表达活化和抑制性受体,以及黏附受体。这些NK细胞受体充当感觉系统,并且此类受体的参与与随后的下游信号的平衡决定了细胞反应。
活化受体
成熟的循环性NK细胞(人:CD56+,小鼠:CD49b+)组成性地表达多种活化受体(表3)。NK细胞在免疫细胞中的独特之处在于,所有成熟循环NK细胞都组成性地表达FCRγ、CD3ζ和DAP12 I型跨膜锚定蛋白,这些蛋白以二硫键结合型的同源二聚体或异源二聚体(在FCRγ和CD3ζ情况下)的形式存在。最重要的是,这些蛋白质在其胞浆区含有免疫受体酪氨酸基活化基序(ITAMS)——由序列(D/E)XXYXX(L/I)X6-8YXX(L/I)定义,其中X代表任意氨基酸,斜杠分开可能占据一个给定位置的替代氨基酸,X6-8表示两个YXX(L/I)元素之间的任意6-8个氨基酸。DAP12和FCRγ含有一个ITAM,CD3ζ每个链含有三个ITAM。在这些蛋白质的短胞内结构域中没有其他已知信号基序,而ITAM酪氨酸残基的突变破坏了其信号功能。 受体与配体结合后,再通过这些含含ITAM的分子促进下游信号传导。NK受体活化时,ITAM被Src激酶磷酸化,从而允许酪氨酸激酶Syk与Zap70结合并活化后者。
激活NK受体的一个重要家族是自然细胞毒性受体(NCR),包括NKp30、NKp44和NKp46。受到刺激时,这些受体向NK细胞传递有效信号,最终溶解有害细胞并生成炎性细胞因子(如IFNγ)。NCR表达于成熟的循环NK细胞,在控制各种病毒感染和癌症方面起着关键作用。
第二个重要活化受体NKG2D的独特之处在于,在人NK细胞上表达时,其与胞内衔接蛋白DAP10相关联以启动不同的信号级联。DAP10含有一个YINM基序,能与PI3K结合并活化它。此外,DAP10能识别Vav1,而Vav1与Grb2相关。NKG2D从最早的NK细胞前体阶段开始表达,除了在溶细胞活性中起作用外,NKG2D还参与诱导其他激活性NK受体的上调。
表 3.NK细胞活化受体。
| 受体 | 配体 | 胞内衔接 | 物种 |
|---|---|---|---|
| KIR2DS1 | HLA-C | DAP12 | H |
| KIR2DS2 | 病毒解旋酶 | DAP12 | H |
| KIR2DS4 | 病毒解旋酶,HLA-Cw4 | DAP12 | H |
| NKG2C/E/H | HLA-E | DAP12 | H, M |
| NKG2D | MICA,MICB,ULBP1 | DAP10 | H, M |
| CD16 | IgG | CD3ζ/FCRγ | H, M |
| NKp46/LY94 | 病毒HA | CD3ζ/FCRγ | H |
| CD122 | IL-2,IL-15 | SHC1 | H, M |
| NKp44 | 病毒HA | DAP12 | H |
| 名词缩写表:DAP12,12 kD的DNAX活化蛋白;FCRγ,IgE受体Ig的Fc片段;HA,血凝素;H,人;HLA,人白细胞抗原;IL,白细胞介素;KLRG,杀伤细胞免疫球蛋白样受体;M,小鼠;MICA,主要组织相容性复合体(MIC)I类链相关蛋白A;MICB,主要组织相容性复合体(MHC)I类链相关蛋白B;NKP,自然杀伤细胞祖细胞;NKG,自然杀伤细胞群;SHC1,SHC衔接蛋白1;ULBP1,UL16结合蛋白1。 | |||
抑制性受体
NK细胞抑制性受体(表4)让NK细胞维持在非活性状态。一些NK抑制性受体对MHC I类分子具有特异性,而另一些则可以结合非MHC配体。其中一些NK抑制性受体(如杀伤细胞免疫球蛋白样受体(KIR)和白细胞免疫球蛋白样受体(LILR))属于免疫球蛋白超家族的单体I型糖蛋白,而Ly49和CD94-NKG2A受体等其他受体则是具有C型类凝集素支架结构的II型糖蛋白。所有抑制性受体在其胞浆区都含有一个共同的免疫受体酪氨酸抑制基序(ITIM)。
表 4.NK细胞抑制性受体。
| 受体 | 配体 | 物种 |
|---|---|---|
| KIR2DL1/2/3 | HLA-C | H |
| KIR3DL1/2 | HLA-A/C | H |
| NKG2A/B | HLA-E | H,M |
| LIR1 | HLA 1类 | H |
| SIGLEC3/7/9 | 唾液酸 | H |
| KLRG1 | 钙粘蛋白 | H,M |
| 名词缩写表:H,人;HLA,人白细胞抗原;IL,白细胞介素;KLRG,杀伤细胞免疫球蛋白样受体;LIR,白细胞免疫球蛋白样受体;M,小鼠;NKG,自然杀伤细胞群;SIGLEC,唾液酸结合性免疫球蛋白样凝集素 | ||
黏附受体
大多数NK细胞驻留在脉管系统中,因此它们必须发生外渗并迁移到炎症、感染或肿瘤发生的部位。黏附受体(表5)对于这一过程至关重要,在NK细胞活化后,这些受体的表达增加。
表 5.NK细胞黏附受体。
| 受体 | 配体 | 物种 |
|---|---|---|
| LFA2 | CD48、CD58 | H, M |
| LFA1 | ICAM-1 | H, M |
| Mac1 | ICAM-1 | H, M |
| CD56 | N-CAM | H |
| CD61 | 纤连蛋白 | H, M |
| 名词缩写表:CD,分化簇;ICAM,细胞间黏附分子;LFA,淋巴细胞功能相关抗原;H,人;M,小鼠;Mac1,巨噬细胞-1抗原。 | ||
NK细胞活性调节
在免疫监视过程中,NK细胞不断与其他细胞接触。NK细可以诱导病毒感染的细胞和肿瘤细胞的细胞溶解活性(无需预先敏化或活化),因此杀伤与否取决于NK细胞表面活化受体和抑制性受体的信号平衡。如上文“NK细胞教育”章节所述,NK细胞与“自身”细胞相互作用,学习如何识别这些细胞,这种相互作用是由那些与健康细胞中MHC(HLA)I类分子特异性结合的NK受体的抑制信号介导的(图2)。当MHC I类分子与潜在的靶细胞结合但无任何活化信号的情况下,NK细胞将该细胞识别为“自身免疫”,并通过ITIM介导的信号减弱细胞溶解活性。当MHC I类分子在肿瘤或病毒感染细胞上出现缺失或下调时(“丧失自我”),抑制性受体信号丢失,导致NK细胞活化和随后的细胞溶解活性。当NK细胞活化受体从靶细胞表达的配体接收活化信号以对病毒感染或肿瘤发生作出反应时,“自我诱导”杀伤过程发生。这种活化信号将优先于抑制信号,导致NK细胞活化和随后的细胞溶解活性。
图 2.NK细胞活化。与邻近细胞相互作用后各种通路(抑制和活化)的整合控制着调节NK细胞活化的动态平衡,并决定了NK细胞是否活化以杀死靶细胞和生成细胞因子。当NK细胞与表达MHC I类分子的正常健康细胞相互作用时,会出现“自我免疫”。当NK细胞与不表达MHC I类分子(因病毒感染或肿瘤发生)的细胞相互作用时,会发生“丧失自我”。这种“自身”抑制信号缺乏会促进NK介导的细胞溶解活性。当细胞表达与活化受体相互作用的配体(如病毒抗原)时,会出现“自我诱导”。这种活化信号将优先于任何抑制信号,并促进NK细胞介导的细胞溶解活性。名词缩写表:MHC,主要组织相容性复合体;MICA/B,主要组织相容性复合体(MHC)I类链相关蛋白A/B。
NK细胞介导的杀伤
NK细胞主要存在于外周循环,它们必须离开脉管系统才能遇到潜在的靶细胞。病毒感染细胞或肿瘤细胞释放的趋化因子会引发血管内皮炎症,内皮环境的改变可引起NK外渗和向趋化因子释放部位迁移。循环中的NK细胞停滞、跨内皮迁移(TEM)、趋化性、炎症部位趋触性、以及炎症部位黏附性均由β1和β3整合素介导。在炎症或肿瘤发生部位,NK细胞通过整合素(尤其是LFA-1)之间的相互作用与潜在靶细胞进行相互作用。
在与潜在靶细胞相互作用期间,NK细胞受体库通过抑制与活化信号的平衡来决定相互作用的结果。如果NK细胞的信号平衡有利于活化,则NK细胞继续进行信号转导和细胞结构的改变,这是NK细胞介导杀伤所必需的。当NK细胞与潜在靶细胞松散接触时,就会发生这种信号转导。做出杀伤决定时,NK细胞牢固地附着在靶细胞上。NK活化受体介导的信号会促进整合素LFA-1(引起整合素聚集和信号转导)由内向外进行信号转导。LFA-1介导的附着诱导肌动蛋白细胞骨架重组,在NK与靶细胞之间形成紧密的溶解性突触(图3)。随后MTOC极化到溶解性突触且微管蛋白出现重组和组装,使溶解颗粒分泌到溶解突触中(图4)。溶解颗粒聚合和极化是NK细胞在实现细胞毒性之前易受抑制信号影响的最后一步。在极化到靶细胞后以及脱粒前,含溶解颗粒的穿孔素和颗粒酶B位于溶解突触处,并与质膜融合。穿孔素被释放,并诱导靶细胞的膜翻转和快速凋亡。
颗粒酶的作用
颗粒酶(颗粒分泌酶)储存在自然杀伤(NK)细胞和细胞毒性淋巴细胞(CTL)溶酶体颗粒中,属于丝氨酸蛋白酶家族。颗粒酶对于诱导靶细胞凋亡至关重要,能分裂细胞内底物,触发许多凋亡通路以确保靶细胞死亡。此外,颗粒酶在抗病毒、肿瘤和胞内细菌免疫方面也发挥着重要作用。近期研究表明,颗粒酶可在细胞外发挥作用(导致组织和血管完整性破坏),这意味着颗粒酶参与了许多炎症和年龄相关疾病。该细胞家族正在成为参与免疫功能和监视的一个重要蛋白类群。
颗粒酶A
颗粒酶A是NK细胞毒性和CD8+细胞毒性T细胞颗粒中最丰富的丝氨酸蛋白酶。它不仅激活一种新的细胞程序性死亡通路-即始于线粒体并生成活性氧(ROS),最终活化单链DNA损伤,还靶向其他重要核蛋白进行降解,包括组蛋白、层连蛋白和几个关键的DNA损伤修复蛋白(如Ku70和PARP-1)。颗粒酶A也有促炎活性;其活化IL-1、TNF- α和IL-6,并可能具有其他尚未了解的作用。
颗粒酶B
颗粒酶B(GrB)存在于NK细胞和细胞毒性T细胞的颗粒中。基于在各种细胞毒性T细胞中的mRNA鉴定,颗粒酶B也被称为CGL1(组织蛋白酶G基质-1)和CTLA-1(细胞毒性T淋巴细胞相关丝氨酸酯酶1),但在非细胞毒性淋巴细胞中未被发现。颗粒酶B对于通过细胞凋亡(与细胞毒性T细胞相互作用诱导)快速诱导靶细胞死亡至关重要。颗粒酶B激活细胞内的半胱天冬酶内级联,并最终导致靶细胞杀伤。
颗粒酶K
像颗粒酶A一样,颗粒酶K是一种类胰蛋白酶丝氨酸蛋白酶,具有部分重叠但不相同的底物特异性。虽然颗粒酶K诱导ROS生成,但也可通过Bid-依赖性线粒体损伤诱导半胱天冬酶非依赖性细胞死亡。此外,数据还显示颗粒酶K能结合并剪切p53。据报道,这种剪切会引起肿瘤细胞介导杀伤。通过活化多种细胞死亡通路,杀伤细胞可以更好地保护细胞免受各种病原体和肿瘤侵害。颗粒酶K也显示出促炎潜能,目前已被证明,细胞外形式的颗粒酶K能够通过激活PAR-1诱导人肺成纤维细胞产生细胞因子
图 3.NK细胞中的LFA-1和肌动蛋白重组可引起紧密的溶解突触。NK原代细胞粘附在ICAM-1上,将福尔马林固定的细胞在室温下用0.1% Triton X-100透化5-10分钟并用3% BSA-PBS封闭30分钟。用LFA-1抗体在3% BSA-PBS(按1:20比例稀释)中对细胞进行处理,并在湿室中4℃孵育过夜。用PBST洗涤细胞,后续于常温用Invitrogen山羊抗小鼠IgG二抗(DyLight 488偶联)在PBS中孵育。然后用Invitrogen Alexa Fluor 568 Phalloidin对细胞进行染色。该荧光图像显示一个密集的外周肌动蛋白环与LFA-1接触环共区域,形成一个紧密的溶解突触。
图 4.NK细胞中的微管蛋白重组导致溶解颗粒释放。(A)附着在靶细胞中的NK细胞的透射光图像。(B)NK和靶细胞用Invitrogen CellLight Tubulin-GFP染色并使用Invitrogen LysoTracker Red DND-99孵育,该图显示了微管朝向靶细胞运动的方向(沿微管系统分布有溶解颗粒)。(C)panel B放大图。
15.自然杀伤细胞概述
什么是自然杀伤(NK)细胞?
自然杀伤(NK)细胞可选择性地溶解细胞,而无需事先活化。NK细胞属于天然淋巴细胞(ILC),天然淋巴细胞作为天然免疫系统的一部分,对于免疫监视和随后的宿主防御病毒感染和癌细胞至关重要。在人体中,NK细胞占循环淋巴细胞的8-20%;在实验室的近交系小鼠中,NK细胞占脾脏和骨髓淋巴细胞的2-5%。与其他淋巴细胞(包括B细胞、T细胞和自然杀伤T(NKT)细胞)不同,NK细胞不表达克隆性B细胞受体或T细胞受体/ CD3ε复合体等抗原特异性受体。相反,NK细胞以抗原非依赖性方式(通常不会生成免疫记忆或长期保护性免疫)发挥作用。近期研究表明,NK细胞是癌症治疗的潜在治疗靶点。
NK细胞发育
人NK细胞发育
人NK细胞在骨髓(BM)和包括扁桃体、脾脏和淋巴结在内的次级淋巴组织(SLT)中发育及成熟。细胞发育分为六个不同阶段(表1)。第1阶段只发生在骨髓,而第2-6阶段可发生在骨髓或次级淋巴组织中。造血干细胞发育成具有淋巴样或髓样偏向的多能祖细胞(MPP)。MPP细胞将生成一个淋巴样祖细胞,该细胞首先发育成NK前体细胞,然后发育成未成熟NK细胞,最后发育为成熟NK细胞。NK前体细胞(NKP)只能分化为成熟NK细胞,而不能分化为T细胞、B细胞、髓样细胞或红系细胞[1]。人NK细胞发育阶段主要基于CD34、CD117、CD56和CD94的表达水平。CD56表达增加是NK成熟的关键,紧随其后的是CD94/NKG2A表达。此外,白细胞介素2/15受体β(CD122)也是NK细胞发育后期的重要标志。
表 1.人NK细胞发育阶段表达的细胞标志物。
| 第1阶段 | 第2阶段 | 第3阶段 | 第4阶段 | 第5阶段 | 第6阶段 | 第7阶段 | 第8阶段 |
|---|---|---|---|---|---|---|---|
| CD34 | CD34 | CD7 | CD7 | CD7 | CD7 | CD7 | CD7 |
| CD133 | CD38 | CD34 | CD45RA | CD244 | CD244 | CD244 | CD244 |
| CD45RA | CD10 | CD45RA | CD244 | CD117dim | CD122 | CD122 | CD122 |
| CD244 | CD133 | CD244 | CD117 | CD122 | NKG2D | NKG2D | NKG2D |
| CD45RA | CD117 | CD122 | NKG2D | CD335 | CD335 | CD335 | |
| CD244 | CD127 | ILR1 | CD161 | CD337 | CD337 | CD337 | |
| CD117 | ILR1 | CD335 | CD335 | NKG2A | NKG2A | NKG2A | |
| CD7 | CD122 | CD337 | CD337 | CD161 | NKP80 | NKP80 | |
| CD127 | CD161 | NKG2A | CD56Hi | CD161 | CD161 | ||
| NKG2D | CD56Hi | NKP80 | CD16 | CD16 | |||
| CD56Low | CD56Low | ||||||
| KIR | |||||||
| CD57 | |||||||
| 缩略语表:CD,分化簇;ILR,IL-1受体;NKG,自然杀伤细胞群。Hi:高表达水平,Low:低表达水平,dim:微弱表达。 | |||||||
小鼠NK细胞发育
小鼠NK细胞在功能方面与人NK细胞相似,但其表达不同的发育标志物并且主要在专门的骨髓龛发育。NK细胞发育始于NK前体细胞(NKP)表达CD122,并经历六个特定阶段(表2)。相继获得NK细胞受体NKG2D/A/C、CD62L、Ly49和CD117(c-Kit)的信号后,小鼠NK细胞可发育成熟。CD51和CD49b的表达定义了小鼠NK细胞成熟的初始阶段,而CD43(白细胞唾液酸蛋白)和CD11b (Mac1)的表达和Ly49受体信号的获得则定义了最终阶段。KLRG1的表达诱导小鼠NK细胞亚群迁移到次级淋巴组织。用CD27和CD11b对小鼠NK细胞进行了额外的功能分类。
表 2.小鼠NK细胞发育阶段表达的细胞标志物。
| NKP | 阶段 A | 阶段 B | 阶段 C | 阶段 D | 阶段 E | 阶段 F |
|---|---|---|---|---|---|---|
| CD27 | CD122 | CD122 | CD122 | CD122 | CD122 | CD122 |
| CD244 | CD27 | CD27 | CD27 | CD27 | CD27 | CD244 |
| CD127 | CD244 | CD244 | CD244 | CD244 | CD244 | NKG2D |
| CD122 | NKG2D | NKG2D | NKG2D | NKG2D | NKG2D | NKG2A/C |
| NKG2A/C | NKG2A/C | NKG2A/C | NKG2A/C | NK1.1 | ||
| NK1.1 | NK1.1 | NK1.1 | NK1.1 | CD62L | ||
| CD43 | CD43 | CD43 | CD62L | CD226 | ||
| CD62L | CD62L | CD62L | CD226 | NCR1 | ||
| CD226 | CD226 | CD226 | NCR1 | CD51 | ||
| NCR1 | NCR1 | CD51 | Ly49 | |||
| CD51 | Ly49 | CD49b | ||||
| Ly49 | CD49b | CD117 | ||||
| CD49b | CD117 | CD11b | ||||
| CD117 | CD11b | KLRG1 | ||||
| 名词缩写表:CD,分化簇;KLRG,杀伤细胞免疫球蛋白样受体;NCR,自然细胞毒作用触发受体;NKP,自然杀伤细胞祖细胞;NKG,自然杀伤细胞群。 | ||||||